Группирование образцов для анализа на SARS-CoV-2 у бессимптомных пациентов

Оригинал: thelancet.com
Тип: Статья
Автор: Stefan Lohse et al.
Опубликовано: Lancet 28 апреля 2020
Перевод: Анна Ковалева, Фонд профилактики рака
Продолжающаяся пандемия коронавирусной болезни (COVID-19) представляет собой существенный вызов для системы здравоохранения и инфраструктуры. Метод ОТ-ПЦР, который используется для подтверждения инфекции, является ключевым для сдерживания распространения вируса, потому что инфекция может протекать бессимптомно, несмотря на высокую вирусную нагрузку. Для обеспечения мер в области здравоохранения, таких как выявление случаев заболевания и изоляция, в т.ч. работников здравоохранения [1], необходимы достаточные возможности молекулярной диагностики.
Протокол РНК ОТ-ПЦР анализа на острый респираторный синдром коронавируса 2 (SARS-CoV-2) стал доступен в уже самом начале пандемии, хотя инфраструктура лабораторий была ограничена, а в некоторых местах и перегружена [2]. Мы предлагаем стратегию тестирования, которую легко имплементировать и которая позволит расширить возможности доступной лабораторной инфраструктуры и наборов для взятия анализов, когда необходимо протестировать большое количество пациентов без симптомов. Мы представили метод группирования образцов до ОТ-ПЦР амплификации, когда обработка индивидуальных результатов инициируется тольков случае позитивных результатов группового тестирования, существенным образом снижая количество необходимых тестов.
Вирусная нагрузка в период симптоматического протекания инфекции SARS-CoV-2 исследована Zou с соавторами [3]. Чтобы проанализировать эффект от группирования образцов на чувствительность ОТ-ПЦР, мы сравнили порог цикла значений (Ct) в группах образцов с Ct в индивидуальных образцах, показавших положительный результат.
Мы выделили РНК с щеточек eSwab (Copan Italia, Брешия, Италия), используя инструмент NucliSens MAG (bioMeriéux Deuchland, Нюртинген, Германия), следуя инструкциям производителя. Для ПЦР амплификации использованы наборы RealStar SARS-CoV-2 RT-PCR 1.0 RUO (Altona Diagnostics, Гамбург, Германия) на Light Cycler 480 II Real-Time PCR Instrument (Roche Diagnostics Deutschland, Мангейм, Германия) согласно инструкциям производителя.
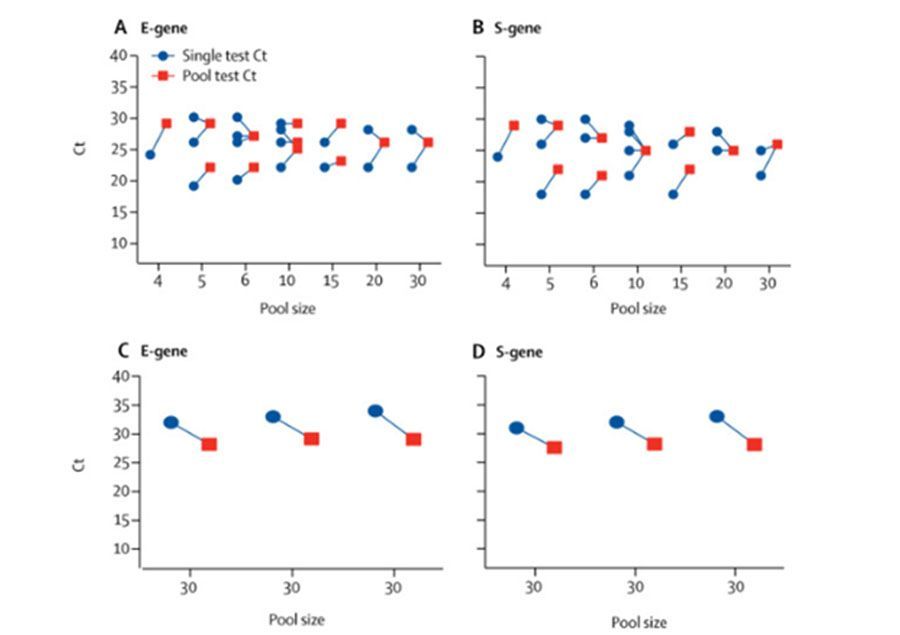
Наши результаты показали, что при размере группы от 4 до 30, порог цикла значений для позитивных групп был между 22 и 29 для пробы гена белка оболочки (E-гена) и между 21 и 29 для пробы на ген белка-шипа (S-ген). Ct значений был ниже в повторных позитивных индивидуальных образцах (рисунок А, В). Ct значений в пробах на E-ген и S-ген в группе и индивидуальных позитивных образцах был ниже 30, что часто квалифицируется как позитивный. Разница в Ct значений между групповым анализом и индивидуальным позитивным анализом (Ct группа – Ct позитивный образец) была в диапазоне до пяти. Даже если Ct значений составлял до 34, позитивные группы также было легко идентифицировать (рисунок C, D). Подгруппы могут помочь еще больше оптимизировать ресурсы, когда превалентность инфекцииявляется низкой. Создание группы из 30 образцов из подгрупп по 10 образцов помогает снизить необходимость повторного тестирования. Если большая группа показывает положительный результат, проводится повторный анализ каждой подгруппы, и затем только тестирование индивидуальных образцов в позитивной подгруппе. В наших анализах в период с 13 по 21 марта тестирование 1191 образцов потребовало использования только 267 тестов и позволило выявить 23 положительных анализа (превалентность 1·93% ). Уровень положительных анализов в нашем институте в этот период составлял 4·24%.
Рис. Значение Ct в индивидуальных и групповых образцах.
Абсолютный Ct значений позитивных групп (13 из 164 протестированных групп) в соотношении к размеру групп и соответствующий Ct значений в индивидуальных образцах для E-ген проб (А) и для S-ген проб (В). Абсолютный Ct значений был ниже 30 для всех размеров групп. Три позитивных индивидуальных образца с Ct значений выше 30 были перемещены в группы с негативными значениями и протестированы с Е-ген (С) и S-ген (D) пробами. Мы предполагаем, что Ct значений у групповых образцов ниже, чем у индивидуальных из-за наличия эффекта переноса более высокого содержания РНК в группах. Соединительные линии показывают позитивные индивидуальные образцы и соответствующие группы. Ct=порог цикла. E-gene=ген белка оболочки. S-gene=ген белка-шип.
Эти данные показывают, что группирование до 30 образцов в группу может увеличить потенциал тестирования при существующем уровне оборудования и количестве наборов для взятия образцов и при этом определять позитивные образцы с высоким уровнем точности. Нужно заметить, что пограничные индивидуальные позитивные образцы могут не определяться в больших группах. Такие образцы можно наблюдать у выздоравливающих пациентов через 14-21 день после симптомной инфекции. Размер группы можно подстраивать под сценарии различных инфекций и оптимизировать в зависимости от ограничений существующей инфраструктуры.
Мы заявляем об отсутствии конкурирующих интересов. Финансирование обеспечено медицинским центром Саарского Университета.
Примечания
1. Koo JR, Cook AR, Park M et al. Interventions to mitigate early spread of SARS-CoV-2 in Singapore: a modelling study. Lancet Infect Dis. 2020; (published online March 23) doi.org
2. Corman VM, Landt O, Kaiser M et al. Detection of 2019 novel coronavirus (2019-nCoV) by real-time RT-PCR. Euro Surveill. 2020; 252000045
3. Zou L, Ruan F, Huang M et al. SARS-CoV-2 viral load in upper respiratory specimens of infected patients. N Engl J Med. 2020; 382: 1177-1179