Сердечно-сосудистые заболевания, лекарственная терапия и смертность у больных COVID-19

Оригинал: The New England Journal of Medicine
Автор: Mandeep R. Mehra et al.
Опубликовано: 01 мая 2020, NEJM
Перевод: Анна Шестакова, Фонд профилактики рака
ОБНОВЛЕНИЕ ОТ 04.06.2020: отзыв статьи "Сердечно-сосудистые заболевания, лекарственная терапия и смертность у больных COVID-19":
Поскольку всем авторам не был предоставлен доступ к необработанным данным, а необработанные данные не могут быть предоставлены сторонним аудитором, для нас не представляется возможным проверить первичные источники данных, лежащие в основе данной статьи. В связи с этим авторы просят отозвать эту статью и приносят извинения редакторам и читателям журнала за принесенные неудобства.
Абстракт
Актуальность исследования. Коронавирусная болезнь 2019 (COVID-19) может сильнее влиять на людей с сердечно-сосудистыми заболеваниями. В этом клиническом контексте есть опасения относительно потенциального вредного действия ингибиторов ангиотензинпревращающего фермента (АПФ) и блокаторов рецепторов ангиотензина (БРА).
Методы исследования. Используя базу данных наблюдений из 169 больниц в Азии, Европе и Северной Америке, мы оценили взаимосвязь сердечно-сосудистых заболеваний, медикаментозной терапии и смертности в стационаре среди пациентов с COVID-19, которые были госпитализированы в период с 20 декабря 2019 года по 15 марта 2020 года, и были зарегистрированы в реестре Surgical Outcomes Collaborative, как умершие в больнице или выжившие до выписки по состоянию на 28 марта 2020 года.
Результаты исследования. Из 8910 пациентов с COVID-19, у которых статус выписки был доступен во время анализа, в общей сложности 515 умерли в больнице (5,8%) и 8395 дожили до выписки. Факторы, которые, как мы выяснили, независимо связаны с повышенным риском смерти в стационаре: возраст старше 65 лет (смертность 10,0%, против 4,9% среди тех, кому ≤65 лет; отношение шансов 1,93; 95% доверительный интервал [ДИ], 1,60-2,41), ишемическая болезнь сердца (10,2% против 5,2% среди людей без заболевания; отношение шансов 2,70; 95% ДИ от 2,08 до 3,51), сердечная недостаточность (15,3% по сравнению с 5,6% среди людей без сердечной недостаточности; отношение шансов 2,48; 95% ДИ от 1,62 до 3,79), аритмиясердца (11,5% против 5,6% среди лиц без аритмии; отношение шансов 1,95; 95% ДИ от 1,33 до 2,86) хроническая обструктивная болезнь легких (ХОБЛ - 14,2% против 5,6% среди людей без заболевания; отношение шансов 2,96; 95% ДИ от 2,00 до 4,40) и текущее курение (9,4% против 5,6% среди бывших курильщиков и некурящих); отношение 1,79; 95% ДИ от 1,29 до 2,47). Мы не обнаружили повышенного риска внутрибольничной смерти, связанной с применением ингибиторов АПФ (2,1% против 6,1%; отношение шансов 0,33; 95% ДИ от 0,20 до 0,54) или БРА (6,8% против 5,7%; отношение шансов 1,23; 95% ДИ от 0,87 до 1,74).
Заключение. Наше исследование подтвердило предыдущие наблюдения, предполагающие, что основное сердечно-сосудистое заболевание связано с повышенным риском внутрибольничной смерти среди пациентов с COVID-19. Наши результаты не подтвердили предыдущие опасения относительно потенциальной вредной связи ингибиторов АПФ или БРА с внутрибольничной смертью в этом клиническом контексте.
Результаты исследования
Пациенты.
Наше исследование включало 8910 госпитализированных пациентов с COVID-19 из 169 больниц, принятых в период с 20 декабря 2019 г. по 15 марта 2020 г., выписанных живыми или умерших к 28 марта 2020 г. Пациенты, госпитализированные в течение этого времени без завершения курса лечения, не были включены в анализ. Наша выборка состояла из 1536 пациентов (17,2%) из Северной Америки, 5755 (64,6%) из Европы и 1619 (18,2%) из Азии (подробная информация об исследуемой популяции в зависимости от континента, страны и количества больниц представлена в таблице S1 в дополнительном приложении, с полным текстом этой статьи можно ознакомиться на сайте NEJM.org). Средний (± SD) возраст пациентов — 49 ± 16 лет (16,5% пациентов были старше 65 лет), 40,0% пациентов — женщины, 63,5% — белые, 7,9% — афроамериканцы, 6,3% — латиноамериканцы и 19,3% — азиаты.
30,5% пациентов имели гиперлипидемию, 26,3% гипертонию, 14,3% сахарный диабет, 16,8% были бывшими курильщиками и 5,5% курили в настоящее время. Анамнез пациентов: у 11,3% — ишемическая болезнь сердца, у 2,1% — застойная сердечная недостаточность, у 3,4% — аритмия. Другие сопутствующие состояния— ХОБЛ (у 2,5% пациентов) и иммуносупрессивное состояние (2,8%). 8,6% пациентов принимали ингибиторы АПФ, 6,2%— БРА, 9,7% — статины, 5,9% — бета-блокаторы, 3,3% — антиагреганты. Инсулин использовали 3,4% пациентов, а9,6% — другие гипогликемические препараты. Средняя продолжительность пребывания в стационаре составила 10,7 ± 2,7 дня, а общая внутрибольничная смертность — 5,8% (515 из 8910 пациентов) в этой группе пациентов с завершенными исходами. Из пациентов, которые были госпитализированы в отделение интенсивной терапии (ОИТ) в любое время в течение их госпитализации, 24,7% умерли по сравнению с 4,0% пациентов, которые не были госпитализированы в ОИТ.
Анализ выживших в сравнении с умершими больными.
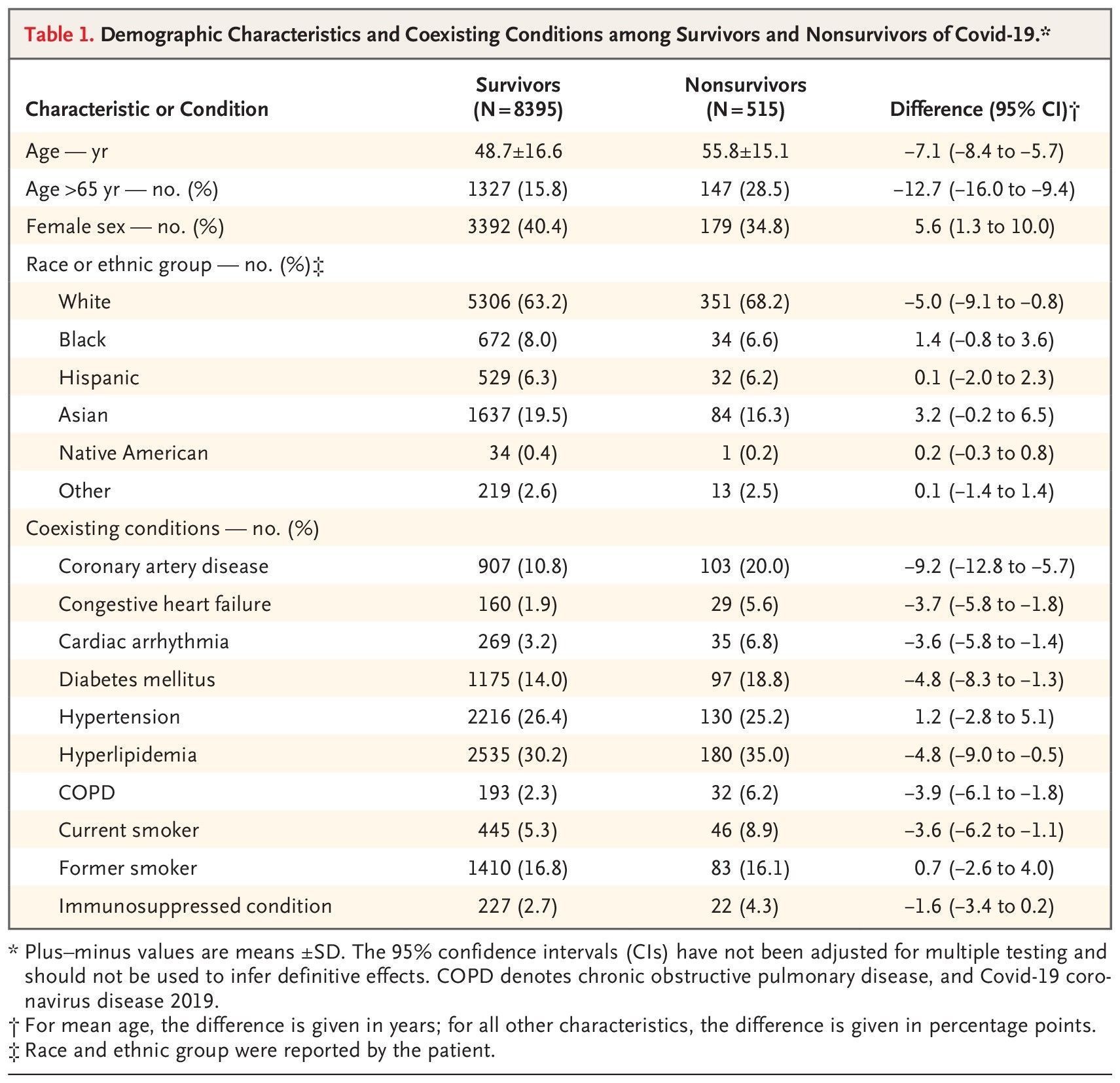
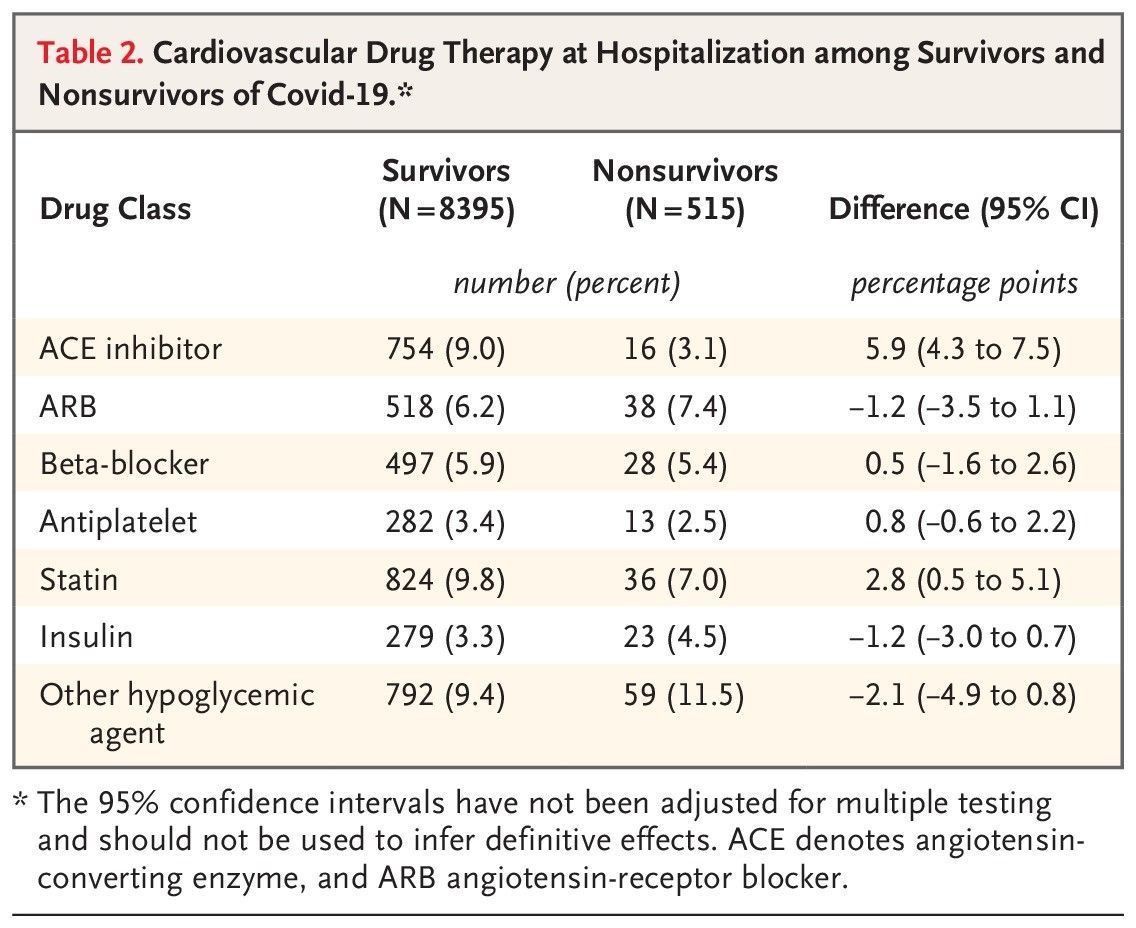
В таблице 1 показано распределение демографических характеристик и сосуществующих условий среди выживших и умерших, а также различия между группами и доверительные интервалы 95%. Не выжившие были пожилыми, чаще белыми и чаще мужчинами, и среди них были больше распространены сахарный диабет, гиперлипидемия, ишемическая болезнь сердца, сердечная недостаточность и аритмия. Умершие пациенты также чаще имели ХОБЛ и стаж курения в прошлом. Ингибиторы АПФ и статины чаще использовались выжившими, чем не выжившими (Таблица 2), связи между выживанием и применением БРА не обнаружено. Продолжительность пребывания в стационаре различалась между выжившими и умершими (10,5 ± 2,5 дня против 7,5 ± 2,8 дня). Когда мы проанализировали данные в соответствии с возрастным децилем, континентом или категорией дохода страны, в которой была расположена больница (с высоким или низким или средним уровнем дохода), то получили аналогичные результаты (рис. S1 и таблицы S2 и S3).
Многопараметрический логистический регрессионный анализ.
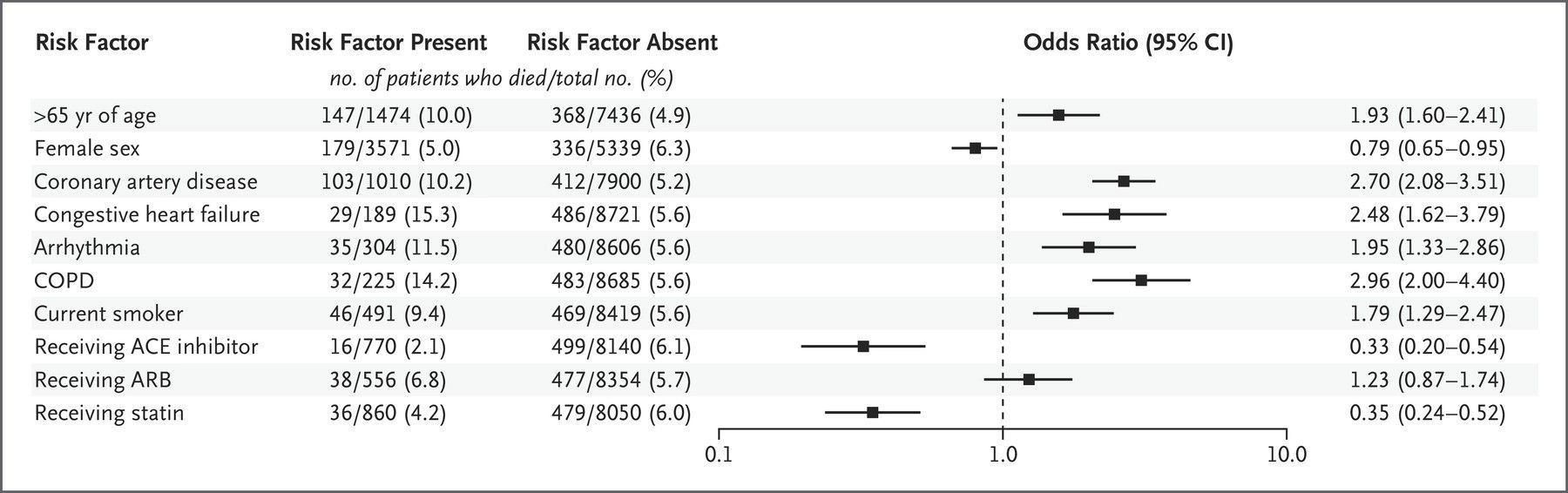
Мы разработали многопараметричесую модель логистической регрессии. Независимые предикторы внутрибольничной смерти, соответствующие им коэффициенты вероятности и 95% доверительные интервалы показаны на рисунке 1. Возраст старше 65 лет, ишемическая болезнь сердца, застойная сердечная недостаточность, аритмия, ХОБЛ и текущее курение связаны с более высоким риском смерти в стационаре. Женский пол, использование ингибиторов АПФ и применение статинов — с большей вероятностью выживания до выписки из больницы, при этом мы не нашли связи данных параметров с применением БРА. Для женского пола отношение шансов на смерть в больнице составляло 0,79 (95% доверительный интервал [ДИ], 0,65–0,95); для тех, кто принимал ингибиторы АПФ — 0,33 (95% ДИ, 0,20 до 0,54); и тех, кто принимал статины — 0,35 (95% ДИ, 0,24 до 0,52). У тех, кто использовал БРА, отношение шансов составило 1,23 (95% ДИ, 0,87-1,74). Наличие или отсутствие иммуносупрессивного состояния, гиперлипидемии или сахарного диабета, раса или этническая группа не были независимыми предвестниками смерти в больнице. Анализ по континентам и категориям доходов в стране (высокий или низкий–средний) соответствовал общим результатам (таблицы S4 и S5). Данные по многопараметрическому логистическому регрессионному анализу с поправкой на возраст и пол приведены в таблице S6.
Дополнительные исследования.
В критическом анализе для оценки потенциального эффекта неизвестного фактора, искажающего результаты, мы подсчитали, что гипотетические ненаблюдаемые двоичные вмешивающиеся факторы с преобладанием 10% в исследуемой популяции должны были бы иметь отношение шансов не менее 10, чтобы наблюдаемые ассоциации для ингибиторов АПФ или статинов имели 95% доверительные интервалы, пересекающие границу отношения шансов 1,0 (таблица S7). Мы также отдельно изучили взаимодействие применения ингибиторов АПФ со смертностью в подгруппе с гипертонией и взаимодействие применения статинов с летальностью в подгруппе с гиперлипидемией. Эти анализы, показанные в таблице S8, согласуются с результатами первичного анализа.
Обсуждение
Наше исследование подтверждает предыдущие сообщения о независимой взаимосвязи старшего возраста, основного сердечно-сосудистого заболевания (ишемическая болезнь сердца, сердечная недостаточность и аритмия), текущего курения и ХОБЛ со смертью от COVID-19. Наши результаты также показывают, что женщины пропорционально чаще, чем мужчины, выживают при инфекции. Не было отмечено ни вредных, ни полезных связей для антиагрегантной терапии, бета-блокаторов или гипогликемической терапии. Мы не смогли подтвердить предыдущие опасения о потенциальной вредной связи между ингибиторами АПФ или БРА с внутрибольничной смертностью.
При вирусных инфекциях, таких как грипп, пожилой возраст ассоциируется с повышенным риском сердечно-сосудистых событий и смерти. В эпидемии тяжелого острого респираторного синдрома 2003 года (SARS, вызванный инфекцией SARS-CoV-1) отмечены половые различия в риске смерти, аналогичные тем, которые мы наблюдали. [1] У женщин более сильный врожденный и адаптивный иммунитет и более высокая устойчивость к вирусным инфекциям, чем у мужчин. [2] Описана более высокая восприимчивость самцов мышей к SARS-CoV-1 и большее накопление макрофагов и нейтрофилов в легких. [3] Овариэктомия или использование антагонистов рецептора эстрогена повышают смертность от инфекции SARS-CoV-1 у самок животных. Кроме того, разница в риске между полами увеличивается с возрастом. [3] Эти результаты могут поддержать наблюдение в нашем исследовании, которое предполагает связь между выживанием и женским полом, независимо от старшего возраста.
Инфекция SARS-CoV-2 является легким заболеванием у большинства людей, но у некоторых COVID-19 прогрессирует до тяжелого респираторного заболевания, которое характеризуется гипервоспалительным синдромом, полиорганной дисфункцией и смертью. [4] В легком вирусный шип-гликопротеин SARS-CoV-2 взаимодействует с ангиотензин-превращающим ферментом-2 (АПФ-2) клеточной поверхности, и вирус проникает внутрь с помощью эндоцитоза. Эндоцитарное событие усиливает активность ADAM(сокращение от англ. A Disintegrin And Metalloproteinase, «дизинтегрин и металлопротеиназа») металлопептидазного домена 17 (ADAM17), который отщепляет АПФ-2 от клеточной мембраны. Это приводит к потере АПФ-2-опосредованной защиты от эффектов активации тканевой ренин-ангиотензин-альдостероновой системы, опосредующей высвобождение провоспалительных цитокинов в кровоток. [5] Стресс от критических заболеваний и воспалений может объединиться, дестабилизируя уже существующие сердечно-сосудистые заболевания. Дисфункция эндотелиальных клеток сосудов, связанная с воспалением депрессия миокарда, стрессовая кардиомиопатия, прямая вирусная инфекция сердца и его сосудов или ответ организма могут вызывать или усугубить сердечную недостаточность, связанную со спросом ишемию, и аритмии. [6] Эти факторы могут лежать в основе наблюдаемой связи между сердечно-сосудистыми заболеваниями и смертью у больных COVID-19.
Использование ингибиторов АПФ или статинов было связано с лучшей выживаемостью среди пациентов с COVID-19. Однако эти связи следует рассматривать с особой осторожностью. Поскольку наше исследование не было рандомизированным, контролируемым испытанием, мы не можем исключать возможность искажения результатов. Кроме того, мы исследовали взаимосвязь между многими переменными и внутрибольничной смертью, и первичная гипотеза не была заранее определена; эти факторы увеличили вероятность обнаружения случайных связей. Следовательно, не нужно выводить причинно-следственную связь между лекарственной терапией и выживанием. Эти данные также не дают информации о потенциальном эффекте применения ингибиторов АПФ или терапии статинами у пациентов с COVID-19, у которых нет соответствующих показаний. Потребуются рандомизированные клинические испытания для оценки роли ингибиторов АПФ и статинов, прежде чем можно будет прийти к какому-либо заключению относительно потенциальной пользы от этих агентов у пациентов с COVID-19.
В этом многонациональном обзорном исследовании с участием пациентов, госпитализированных с COVID-19, мы подтвердили предыдущие наблюдения, предполагающие, что основное сердечно-сосудистое заболевание независимо связано с повышенным риском смерти в стационаре. Мы не смогли подтвердить предыдущие опасения относительно потенциальной пагубной связи ингибиторов АПФ или БРА с внутрибольничной смертностью в этом клиническом контексте.
Table 1. Demographic Characteristics and Coexisting Conditions among Survivors and Nonsurvivors of Covid-19.
Table 2. Cardiovascular Drug Therapy at Hospitalization among Survivors and Nonsurvivors of Covid-19.
Figure 1. Independent Predictors of In-Hospital Death from Multivariable Logistic-Regression Analysis.
Показаны числа и проценты пациентов с каждым фактором риска смерти (фактор риска присутствует) и пациентов без каждого фактора риска, который умер (фактор риска отсутствует). 95% доверительные интервалы (ДИ) отношений шансов не были скорректированы для многократного тестирования и не должны использоваться для определения окончательных эффектов. ACE обозначает ангиотензинпревращающий фермент, блокатор рецепторов ангиотензина ARB и хроническую обструктивную болезнь легких ХОБЛ.
Список использованной литературы:
- Karlberg J, Chong DSY, Lai WYY. Do men have a higher case fatality rate of severe acute respiratory syndrome than women do? Am J Epidemiol 2004;159:229- 31.
- Klein SL, Flanagan KL. Sex differences in immune responses. Nat Rev Immunol 2016;16:626-38.
- Channappanavar R, Fett C, Mack M, Ten Eyck PP, Meyerholz DK, Perlman S. Sex-based differences in susceptibility to severe acute respiratory syndrome coronavirus infection. J Immunol 2017;198: 4046-53.
- Siddiqi HK, Mehra MR. COVID-19 illness in native and immunosuppressed states: a clinical-therapeutic staging proposal. J Heart Lung Transplant 2020;39:405-7.
- Wang K, Gheblawi M, Oudit GY. Angiotensin converting enzyme 2: a double-edged sword. Circulation 2020 March 26 (Epub ahead of print).
- Mehra MR, Ruschitzka F. COVID-19 illness and heart failure: a missing link? JACC Heart Fail (in press).