Ретроспективное когортное исследование терапии метилпреднизолоном у пациентов с тяжелой формой пневмонии COVID-19

Тип: Письмо в редакцию / информационное сообщение
Специальность: Терапия; Лечение COVID-19
Автор: Yin Wang, Weiwei Jiang, Qi He, Cheng Wang, Baoju Wang, Pan Zhou, Nianguo Dong & Qiaoxia Tong
Опубликовано: Signal Transduction and Targeted Therapy
Перевод: Злотникова Екатерина, Фонд профилактики рака
Заболевание, вызванное коронавирусом 2019 года (COVID-19), впервые было зарегистрировано в конце декабря 2019 года в Ухане, Китай. В мире зарегистрировано более 1 800 000 подтвержденных случаев 1. Патологический процесс тяжелой пневмонии COVID-19 представляет собой воспалительную реакцию, характеризующуюся разрушением глубоких дыхательных путей и альвеол 2. В настоящее время считается, что повреждение легких связано не только с прямым воздействием вируса, но также с иммунным ответом, триггером которого является COVID-19, что приводит к активации иммунных клеток для высвобождения большого количества про- и противовоспалительных цитокинов. Гистологическое исследование показало диффузное альвеолярное повреждение и муцинозный экссудат, который похож на острый респираторный дистресс-синдром 2. Обострение симптомов всегда происходит в течение 5–7 дней после начала заболевания у пациентов с пневмонией COVID-19. Тяжелые случаи быстро развиваются до острой дыхательной недостаточности 3. Следовательно, важно усилить лечение, чтобы подавить провоспалительный ответ и контролировать цитокиновый шторм на этой стадии. Метилпреднизолон - это классические иммуносупрессивные препараты, которые важны для остановки или задержки развития пневмонии. Они показали свою эффективность для лечения острого респираторного дистресс-синдрома (ARDS).
В последнем исследовании Wu и др. 4 обнаружили что применение метилпреднизолона, по-видимому, снижает риск смерти у пациентов с пневмонией COVID-19 и острым респираторным дистресс-синдромом, однако, из тех пациентов кто получал лечение метилпреднизолоном, 23 из 50 пациентов умерли. Это достаточно высокий уровень смертности порядка 50%, поэтому, с точки зрения показаний, сроков, дозировки и продолжительности применение метилпреднизолона требует дальнейшее изучение вопроса. В другом исследовании Zhou и др. 5 показали потенциальные преимущества лечения низкими дозами кортикостероидов у подгруппы пациентов в критическом состоянии с пневмонией COVID-19, однако данные ограничены только 15 пациентами при отсутствии контрольной группы. Несмотря на то, что это важный вопрос, связанный с проблемами лечения тяжелой пневмонии COVID-19, клиническая применимость метилпреднизолона должна быть изучена дополнительно из-за оставшихся без ответа вопросов. Чтобы решить эту проблему, мы провели ретроспективное когортное исследование, сравнивая клинические результаты пациентов с пневмонией, вызванной COVID-19, с или без лечения метилпреднизолоном.
Мы изучили 46 тяжелых пациентов с пневмонией COVID-19 в изолированном крыле Union Hospital of Huazhong University of Science and Technology, Юхань, Китай, в период с 20 января по 25 февраля 2020. Клиническая классификация основана на плане диагностики и лечения коронавирусной пневмонии (пробная версия 5), разработанном Национальным комитетом здравоохранения Китайской Народной Республики. Случай определялся как тяжелый случай при выполнении любого из следующих критериев: (1) дыхательная недостаточность, частота дыхания в минуту ≥ 30; (2) в состоянии покоя значение сатурации кислородом ≤ 93%; (3) парциальное давление кислорода в артериальной крови/концентрация кислорода ≤ 300 мм рт. ст.
Возраст, пол, сопутствующие заболевания, клинические и лабораторные параметры этих пациентов при поступлении приведены в дополнительной таблице. S1. Три (5,4%) пациента умерли во время госпитализации, а остальные 43 пациента были успешно выписаны. Кислородная терапия, противовирусная терапия (а-интерферон, Калетра [лопинавир/ритонавир]), иммуноферментная терапия (тимозин), профилактика бактериальной инфекции, облегчение кашля, устраняющее мокроту, и нутритивная поддержка использовались для всех 46 пациентов; тогда как 26 из них дополнительно получали лечение метилпреднизолоном в низких дозах в дозировке 1–2 мг/кг/сут в течение 5–7 дней путем внутривенной инъекции. Конкретную дозировку и продолжительность применения метилпреднизолона для пациентов определяли в соответствии с клиническими проявлениями, числом лейкоцитов, числом лимфоцитов, индексом воспаления и диапазоном поражения. Не было значительных различий в возрасте, поле, сопутствующих заболеваниях, клинических или лабораторных параметрах между двумя группами (дополнительная таблица S1).
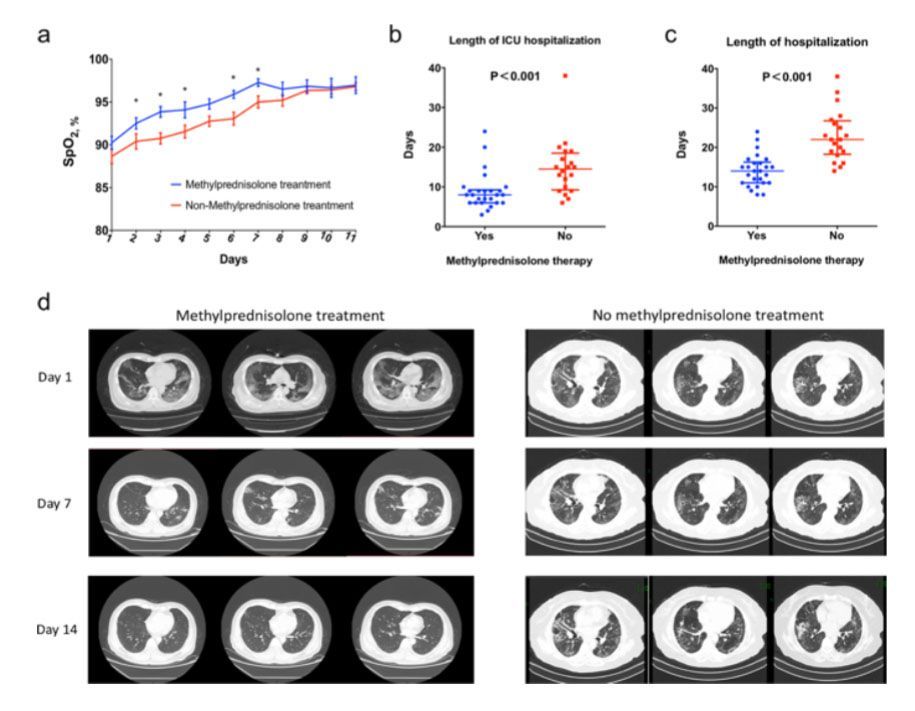
Медианное значение SpO2 было схожим в обеих группах. Все 46 пациентов получали кислородную терапию. Динамическое изменение SpO2 показано на рис. 1a. Пациенты, получавшие лечение метилпреднизолоном имели более быстрое улучшение показателя SpO2. Кроме того, пациенты без лечения метилпреднизолоном имели значительно более длительный интервал применения дополнительной кислородной терапии, чем пациенты с лечением метилпреднизолоном. (8 дней [межквартильный диапазон (IQR) 7–10] против 14 дней (IQR 10–16); P <0,001). Что касается наиболее интенсивного уровня кислородной поддержки, у пациентов, получавших лечение метилпреднизолоном, вероятность развития состояния до необходимости искусственной вентиляции легких была ниже (P = 0.05); 35% (7/20) пациентов без лечения метилпреднизолоном достигли необходимости ИВЛ (5 неинвазивная вентиляция, 2 инвазивная вентиляция), ЭКМО не применялась; тогда как в группе получавших лечение метилпреднизолоном только 11.5% (3/26) пациентов достигли необходимости ИВЛ (2 неинвазивная вентиляция, 1 инвазивная вентиляция, ЭКМО не применялась).
Лабораторное исследование проводилось каждые 3 дня и лечение метилпреднизолоном сочеталось с более быстрым снижением уровня С-реактивного белка и интерлейкина-6 (рис. 1c, d), тогда как по другим показателям воспаления значимой разницы обнаружено не было (дополнительный рис. S1). Два пациента умерло в группе с лечением метилпреднизолоном и один в группе без лечения метилпреднизолоном. Значимой разницы в уровне смертности между двумя группами не обнаружено (P = 0.714). Кроме того, длительность госпитализации в ОРИТ была значительно короче у пациентов, получавших лечение метилпреднизолоном. (8 дней [IQR 6–9] и соответственно 15 дней [IQR 9–19]; P < 0.001, Рис. 1b) и также длительность госпитализации (14 дней [IQR 11–16] и соответственно 22 дня [IQR 18–26]; P < 0.001, Рис. 1c). С точки зрения КТ грудной клетки на 7 и 14 день степень абсорбции фокуса была значительно лучше у пациентов с лечением метилпреднизолоном (Рис. 1d).
Осложнения, вызванные лечением метилпреднизолоном, являются еще одной серьезной проблемой. Наиболее распространенным осложнением, вызванным метилпреднизолоном, является вторичная инфекция. По нашему опыту, когда вторичная инфекция возникает у тяжелых пациентов с пневмонией COVID-19, следует немедленно добавить антибактериальные препараты с соответствующей чувствительностью и в полной дозировке. Во-вторых, использование иммунорегуляторов (иммуноглобулина человека) может улучшить иммунную функцию пациентов. По нашему опыту, человеческий иммуноглобулин обычно использовался у критических пациентов с дозировкой 10–20 г/день в течение 7–10 дней в качестве импульсной терапии. В-третьих, тимозин, секретируемый эпителиальными клетками тимуса, может способствовать созреванию Т-лимфоцитов и регулировать функцию клеточного иммунитета. Мы предлагаем использовать тимозин во время госпитализации. Курс лечения можно определить по результатам исследования лимфоцитов. Благодаря мониторингу состояния и адаптации ведения в данной выборке не наблюдалось серьезных осложнений, вызванных лечением метилпреднизолоном.
В заключение, раннее, низкодозированное и краткосрочное применение метилпреднизолона было связано с лучшими клиническими исходами у тяжелых пациентов с пневмонией COVID-19 и должно быть рассмотрено до появления острого респираторного дистресс-синдрома. Тем не менее, в будущих рандомизированных контролируемых исследованиях крайне необходимо подтвердить эти выводы и дополнительно изучить среднесрочные и долгосрочные результаты после выписки.
1. Zhu, N. et al. A novel coronavirus from patients with pneumonia in China, 2019. N. Engl. J. Med. 382, 727–733 (2020).
2. Xu, Z. et al. Pathological findings of COVID-19 associated with acute respiratory distress syndrome. Lancet Respir. Med. 8, 420–422 (2020).
3. Huang, C. et al. Clinical features of patients infected with 2019 novel coronavirus in Wuhan, China. Lancet 395, 497–506 (2020).
4. Wu, C. et al. Risk factors associated with acute respiratory distress syndrome and death in patients with coronavirus disease 2019 pneumonia in Wuhan, China. JAMA Intern. Med. e200994 (2020). [published online ahead of print, 2020 Mar 13].
5. Zhou, W. et al. Potential benefits of precise corticosteroids therapy for severe 2019-nCoV pneumonia. Signal Transduct. Target Ther. 5, 18 (2020).