Ремдесивир для лечения COVID-19: заключительный отчет

Оригинал: The New England Journal of Medicine
Опубликовано: 05 ноября 2020, NEJM
Перевод: Анна Селюта, ФГБУ НМИЦ онкологии им. Н.Н. Петрова, Фонд медицинских решений «Не напрасно!»
Редакция: Евгения Фрей, Фонд медицинских решений «Не напрасно!»
Аннотация
Актуальность проблемы
В настоящее время исследуются несколько препаратов для лечения коронавирусной инфекции 2019 (COVID‑19). Однако ни один противовирусный препарат пока не признан эффективным.
Методы
Мы провели двойное слепое рандомизированное плацебо-контролируемое исследование ремдесивира для внутривенного введения у взрослых пациентов, госпитализированных с COVID‑19 и признаками инфекции нижних дыхательных путей. Пациенты были рандомизированы в две группы. В первой группе пациенты получали ремдесивир (нагрузочная доза 200 мг в 1-й день, затем по 100 мг ежедневно в течение 9 дней), во второй группе пациенты в течение 10 дней получали плацебо. Первичной конечной точкой было время до выздоровления. Выздоровлением считалась либо выписка из больницы, либо продление госпитализации по немедицинским показаниям (например, для контроля инфекции).
Результаты
Рандомизацию прошли 1062 пациента (541 пациент включен в группу ремдесивира, 521 пациент — в группу плацебо). В группе ремдесивира медиана времени до выздоровления составила 10 дней (95 % доверительный интервал [ДИ] 9–11); в группе плацебо — 15 дней (95 % ДИ 13–18). Отношение частот выздоровления составило 1,29; 95 % ДИ 1,12–1,49; P < 0,001 по логранговому критерию). При анализе с использованием модели пропорциональных шансов с порядковой шкалой из 8 категорий (шкала клинического состояния) было обнаружено, что у пациентов, получавших ремдесивир, вероятность клинического улучшения на 15-й день была выше, чем у пациентов, получавших плацебо (отношение шансов [ОШ]к 1,5; 95 % ДИ 1,2–1,9, анализ проводили с поправкой на фактическую тяжесть течения заболевания). Смертность, оцененная по методу Каплана-Майера, на 15-й день составила 6,7 % в группе ремдесивира и 11,9 % в группе плацебо; на 29-й день — 11,4 % в группе ремдесивира и 15,2 % в группе плацебо (отношение рисков [ОР] 0,73; 95 % ДИ 0,52–1,03). Серьезные нежелательные явления были зарегистрированы у 131 из 532 пациентов, получавших ремдесивир (24,6 %), и у 163 из 516 пациентов, получавших плацебо (31,6 %).
Выводы
Наши данные показывают, что ремдесивир сокращает время до выздоровления у взрослых, госпитализированных с COVID‑19 и признаками инфекции нижних дыхательных путей, по сравнению с плацебо. Исследование финансировалось Национальным институтом аллергии и инфекционных заболеваний и другими организациями; Adaptive COVID‑19 Treatment Trial (ACTT-1) ClinicalTrials.gov, NCT04280705.
Введение
Коронавирус тяжелого острого респираторного синдрома-2 (SARS‑CoV‑2) — новый вирус, впервые идентифицированный в декабре 2019 года как причина респираторного заболевания, названного «коронавирусное заболевание 2019», или COVID‑19 [1]. Исследуются несколько препаратов для лечения COVID‑19, но пока ни один противовирусный препарат не признан эффективным [2, 3]. С момента публикации нашего предварительного отчета было показано, что дексаметазон снижает смертность при COVID‑19 (25,7 % в группе стандартной терапии против 22,9 % в группе дексаметазона; P < 0,001), причем максимальный эффект наблюдался у пациентов, находившихся на ИВЛ [4].
Ремдесивир (GS-5734) является ингибитором вирусной РНК‑зависимой РНК‑полимеразы. В условиях in vitro ремдесивир обладает ингибирующей активностью в отношении вирусов SARS‑CoV‑1 и MERS‑CoV (коронавирус ближневосточного респираторного синдрома) [5, 6, 7, 8]. Благодаря способности ингибировать вирус SARS‑CoV‑2 в условиях in vitro ремдесивир признали многообещающим препаратом для лечения COVID‑19 [9]. Кроме того, в исследованиях на приматах терапия ремдесивиром, начатая через 12 часов после инокуляции MERS‑CoV [10, 11], снижала уровни вируса в легких и уменьшала повреждение легких.
Чтобы оценить клиническую эффективность и безопасность потенциальных терапевтических средств среди госпитализированных взрослых с лабораторно подтвержденным COVID‑19, мы разработали адаптивную платформу, предназначенную для быстрого проведения серии рандомизированных двойных слепых плацебо‑контролируемых исследований фазы 3. В данной статье описана первая стадия клинического исследования ACTT-1 (Adaptive Covid‑19 Treatment Trial), в котором ремдесивир сравнивался с плацебо. Это обновленная версия предварительного отчета, составленная после завершения наблюдения.
Результаты
Пациенты
Из 1114 пациентов, оцененных по критериям включения, 1062 прошли рандомизацию; 541 пациент рандомизирован в группу ремдесивира, 521 пациент — в группу плацебо (популяция, сформированная в соответствии с назначенным лечением) (см. рисунок 1). У 159 пациентов (15,0 %) степень тяжести заболевания была определена как легкая или средняя, у 903 пациентов (85, 0%) заболевание было классифицировано как тяжелое. Из всех пациентов, рандомизированных в группу ремдесивира, 531 человек (98,2 %) получили препарат в соответствии с исходным планом. 52 пациента прекратили терапию ремдесивиром до 10 дня из-за развития нежелательного явления или серьезного нежелательного явления (исключая летальный исход), и 10 человек отозвали свое согласие на участие. Из всех пациентов, рандомизированных в группу плацебо, 517 человек (99,2 %) получили плацебо в соответствии с исходным планом. 70 пациентов прекратили прием плацебо до 10 дня из-за развития нежелательного явления или серьезного нежелательного явления (исключая летальный исход), и 14 человек отозвали свое согласие на участие.
Клиническое исследование продолжалось 29 дней. 517 пациентов в группе ремдесивира и 508 пациентов в группе плацебо завершили исследование (включая случаи выздоровления и летального исхода). 14 пациентов, получавших ремдесивир, и 9 пациентов, получавших плацебо, прекратили участие в исследовании до 29-го дня. У 54 пациентов, исходно рандомизированных в страту легкой и средней степени тяжести заболевания, впоследствии заболевание было классифицировано как тяжелое. В результате в страте легкой и средней степени тяжести заболевания остались 105 пациентов, и 957 пациентов были отнесены к страте тяжелого заболевания. Популяция, сформированная согласно фактически полученному лечению, включала 1048 пациентов, получивших назначенную терапию (532 пациента в группе ремдесивира, в том числе один пациент, который был рандомизирован в группу плацебо, но получал ремдесивир, и 516 пациентов в группе плацебо).
Средний возраст пациентов составил 58,9 лет, и 64,4 % пациентов составляли мужчины (таблица 1). Из-за особенностей распространения COVID‑19 79,8 % пациентов включили в исследование в центрах Северной Америки, 15,3 % — в Европе, и 4,9 % в Азии (таблица S1 [см. таблицы с буквой S в дополнительном приложении — прим. перев.]). Всего в исследовании участвовали 53,3 % пациентов европеоидной расы, 21,3 % — негроидной, 12,7 % — азиатской; 12,7 % были отнесены к другим этническим группам, или раса не была указана; 250 пациентов (23,5 %) были испаноязычными или латиноамериканцами. У 25,9 %пациентов на момент включения в исследование имелось одно сопутствующее заболевание, у 54,5 % — два или более. Наиболее распространенными сопутствующими заболеваниями были артериальная гипертензия (50,2 %), ожирение (44,8 %) и сахарный диабет 2 типа (30,3 %).
Медиана количества дней между появлением симптомов и рандомизацией составила 9 (межквартильный интервал [IQR] 6–12) (таблица S2). У 957 пациентов (90,1 %) на момент включения в исследование заболевание было классифицировано как тяжелое. Состояние 285 пациентов (26,8 %) соответствовало категории 7 по шкале клинического состояния; состояние 193 (18,2 %) пациентов — категории 6; состояние 435 (41,0 %) пациентов — категории 5 и состояние 138 (13,0 %) пациентов — категории 4. У 11 пациентов (1,0 %) данные о категории по шкале клинического состояния при включении в исследование отсутствовали; все эти пациенты прекратили участие в исследование до начала лечения. В ходе исследования 373 пациента (35,6 % из 1048 пациентов — популяции, сформированной согласно фактически полученному лечению) получали гидроксихлорохин, а 241 (23,0 %) пациент получали глюкокортикоиды (таблица S3).
Первичная конечная точка
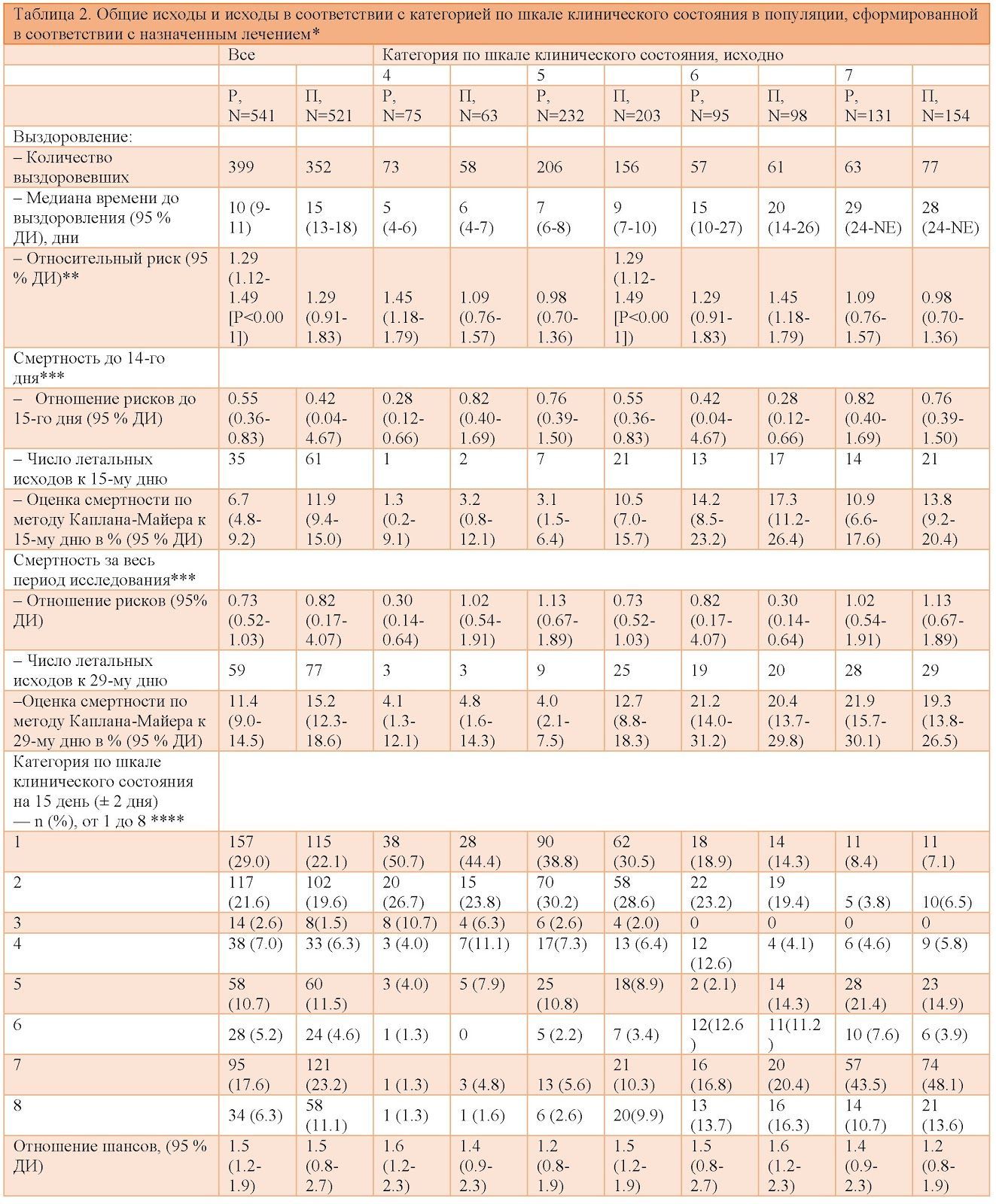
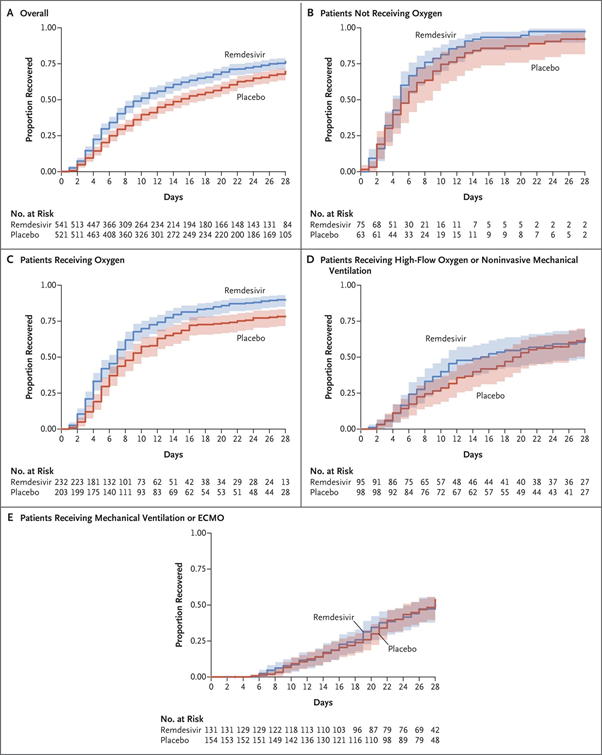
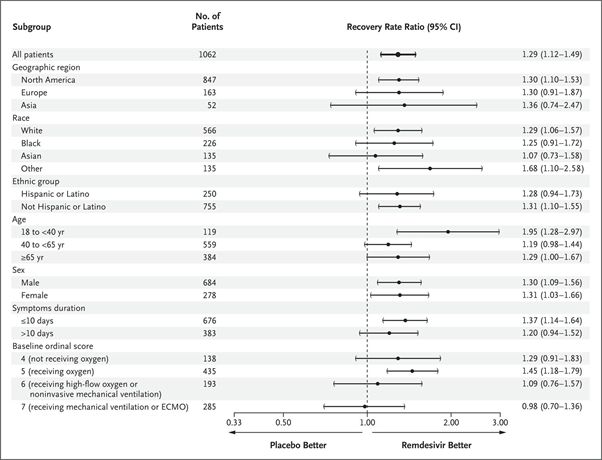
В группе ремдесивира выздоровление наступало быстрее, чем в группе плацебо (медианы составили 10 дней и 15 дней, соответственно; отношение частот выздоровления 1,29; 95 % доверительный интервал [ДИ] 1,12–1,49; P < 0,001) (рисунок 2 и таблица 2). В страте тяжелого заболевания (957 пациентов) медиана времени до выздоровления составила 11 дней по сравнению с 18 днями (отношение частот выздоровления 1,31; 95 % ДИ 1,12–1,52) (таблица S4). Отношение частот выздоровления было максимальным среди пациентов с исходной категорией 5 по шкале клинического состояния (отношение частот выздоровления 1,45; 95 % ДИ 1,18–1,79); среди пациентов с исходной категорией 4 и исходной категорией 6 этот показатель составил 1,29 (95 % ДИ 0,91–1,83) и 1,09 (95 % ДИ 0,76–1,57), соответственно. Для тех, кто при включении в исследование находились на ИВЛ или ЭКМО (категория 7), отношение частот выздоровления составило 0,98 (95 % ДИ 0,70–1,36). Дополнительные результаты анализа, полученные с использованием модели пропорциональных интенсивностей Кокса (в частности, когда номер исходной категории рассматривался как непрерывная переменная), представлены в таблице S11. Мы провели общий анализ, включив в базовую модель исходную категорию в качестве ковариаты. Результаты аналогичны полученным ранее: отношение частот выздоровления 1,26; 95 % ДИ 1,09–1,46). Отношение частот выздоровления у пациентов, прошедших рандомизацию в течение первых 10 дней после появления симптомов, составило 1,37 (95 % ДИ 1,14–1,64). У пациентов, прошедших рандомизацию позднее (более чем через 10 дней после появления симптомов), отношение частот выздоровления равнялось 1,20 (95 % ДИ 0,94–1,52) (рисунок 3). Преимущества ремдесивира были более выраженными на ранней стадии заболевания, но, по данным большинства анализов, сохранялись определенное время (таблица S6).
Анализы чувствительности, в которых данные о пациентах, получавших глюкокортикоиды или гидроксихлорохин, были цензузированы по наиболее раннему сообщению об использовании препаратов, тоже продемонстрировали эффективность ремдесивира. Для пациентов, получавших глюкокортикоиды, получены следующие результаты: 9,0 дней до выздоровления в группе ремдесивира против 14,0 дней в группе плацебо; отношение частот выздоровления 1,28; 95 % ДИ 1,09–1,50. Для пациентов, получавших гидроксихлорохин: 10,0 дней до выздоровления в группе ремдесивира по сравнению с 16,0 днями в группе плацебо; отношение частот выздоровления 1,32; 95 % ДИ 1,11–1,58) (таблица S8).
Основная вторичная конечная точка
Шансы на улучшение категории по шкале клинического состояния на 15-й день в группе ремдесивира были выше, чем в группе плацебо, как было определено с помощью модели пропорциональных шансов (отношение шансов улучшения состояния 1,5; 95 % ДИ 1,2–1,9, с поправкой на тяжесть течения заболевания) (таблица 2 и рисунок S7).
Смертность
Смертность, оцененная по методу Каплана-Майера, к 15-му дню составила 6,7 % в группе ремдесивира и 11,9 % в группе плацебо (отношение рисков 0,55; 95 % ДИ 0,36–0,83); к 29-му дню смертность в группах ремдесивира и плацебо составила 11,4 % и 15,2 %, соответственно (отношение рисков 0,73; 95 % ДИ 0,52–1,03). При этом наблюдались выраженные межгрупповые различия, в зависимости от исходной степени тяжести (таблица 2). Наиболее значительные различия наблюдались в группе пациентов с исходной категорией 5 (отношение рисков 0,30; 95 % ДИ 0,14–0,64). Дополнительные результаты анализа, полученные с использованием модели пропорциональных интенсивностей Кокса, представлены в таблице S11.
Дополнительные вторичные конечные точки
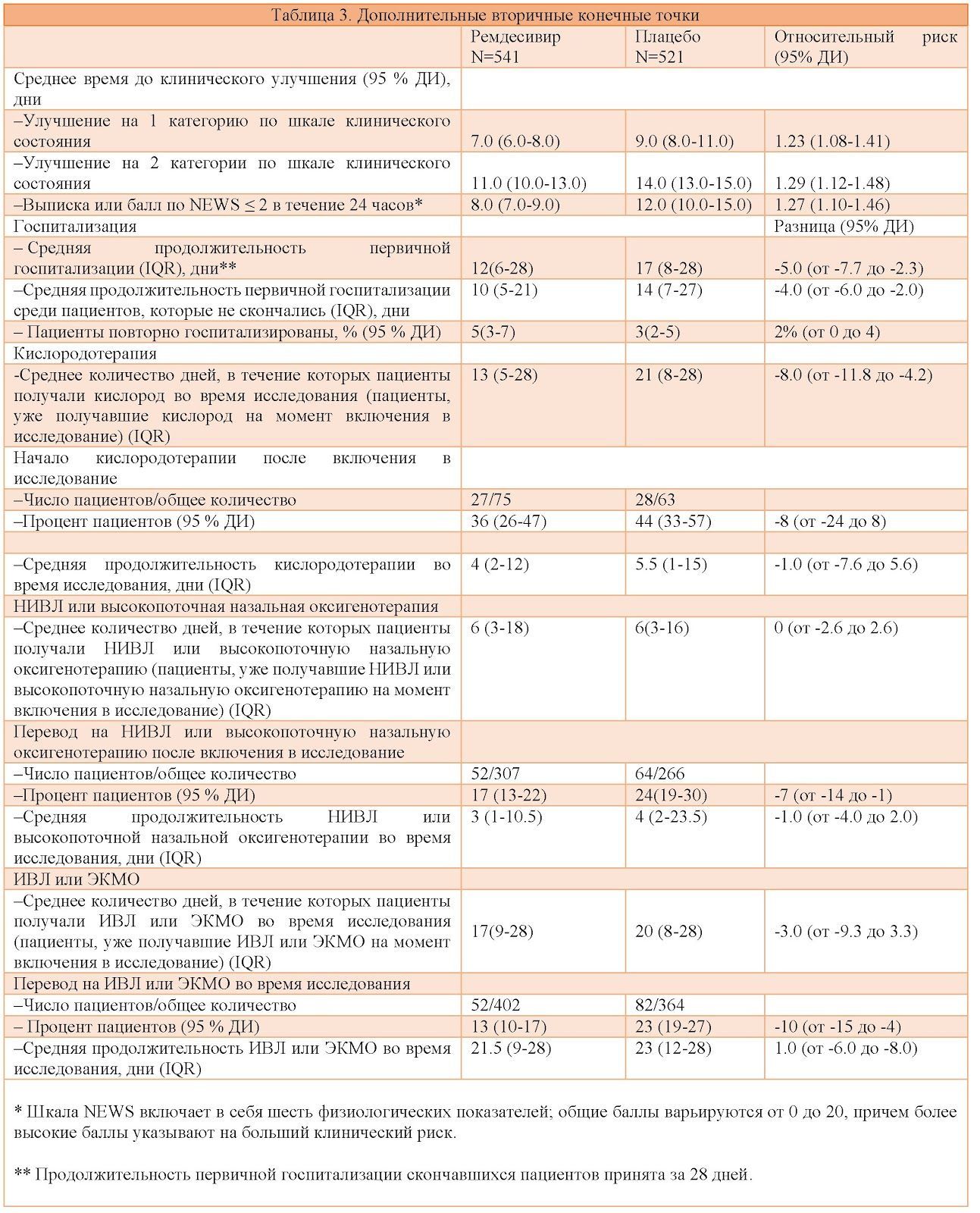
Категория по шкале клинического состояния в группе ремдесивира улучшалась быстрее, чем в группе плацебо. Улучшение на одну категорию: 7 дней и 9 дней, соответственно (медиана времени); отношение частот выздоровления 1,23; 95 % ДИ 1,08–1,41. Улучшение на две категории: 11 дней и 14 дней, соответственно (медиана времени); отношение частот выздоровления 1,29; 95 % ДИ 1,12–1,48 (таблица 3). Время до выписки или до достижения целевых баллов (≤ 2) по шкале NEWS [см. ссылку] в группе ремдесивира было меньше, чем в группе плацебо: 8 дней и 12 дней, соответственно (медиана времени); отношение рисков 1,27; 95 % ДИ 1,10–1,46. Средняя продолжительность первоначальной госпитализации в группе ремдесивира была меньше, чем в группе плацебо: 12 дней и 17 дней, соответственно. При этом 5 % пациентов из группы ремдесивира и 3 % пациентов из группы плацебо были госпитализированы повторно.
Среди 913 пациентов, получавших кислород при включении в исследование, пациенты в группе ремдесивира продолжали получать кислород в течение меньшего количества дней, чем пациенты в группе плацебо (среднее 13 дней и 21 день, соответственно). Частота начала кислородотерапии среди пациентов, которые не получали кислород при включении в исследование, была ниже в группе ремдесивира, чем в группе плацебо: 36 % (95 % ДИ 26–47) против 44 % (95 % ДИ 33–57), соответственно.
Для 193 пациентов, которым при включении в исследование проводилась неинвазивная вентиляция легких (НИВЛ) или высокопоточная назальная оксигенотерапия, средняя продолжительность респираторной поддержки составила 6 дней как в группе ремдесивира, так и в группе плацебо. Среди 573 пациентов, которые при включении в исследование не получали респираторную поддержку (НИВЛ, высокопоточная назальная оксигенотерапия, ИВЛ) или ЭКМО, частота начала неинвазивной респираторной поддержки (высокопоточная назальная оксигенотерапия, НИВЛ) была ниже в группе ремдесивира, чем в группе плацебо: 17 % (95 % ДИ 13–22) против 24 % (95 % ДИ 19–30), соответственно. Среди 285 пациентов, которые при включении в исследовании находились на ИВЛ или ЭКМО, средняя непрерывная продолжительность этих вмешательств была меньше в группе ремдесивира, чем в группе плацебо (17 дней и 20 дней, соответственно). Частота начала ИВЛ или ЭКМО среди 766 пациентов, которым эти вмешательства на момент включения в исследование не проводились, была ниже в группе ремдесивира, чем в группе плацебо: 13 % (95 % ДИ 10–17) против 23 % (95 % ДИ 19–27 ) (таблица 3).
Результаты исследования безопасности
В популяции, сформированной согласно фактически полученному лечению, серьезные нежелательные явления возникли у 131 из 532 пациентов (24,6 %) в группе ремдесивира и у 163 из 516 пациентов (31,6 %) в группе плацебо (таблица S17). В группе ремдесивира наблюдалось 47 случаев дыхательной недостаточности (8,8 % пациентов), включая острую дыхательную недостаточность и необходимость в интубации трахеи; в группе плацебо число случаев дыхательной недостаточности составило 80 (15,5 % пациентов) (таблица S19). Летальные исходы, по мнению исследователей, не были связаны с распределением в группы лечения.
Нежелательные явления 3 или 4 степени возникли на 29-й день или ранее у 273 пациентов (51,3 %) в группе ремдесивира и у 295 пациентов (57,2 %) в группе плацебо (таблица S18). Исследователи сочли, что 41 нежелательное явление связано с применением ремдесивира, а 47 — с плацебо (таблица S17). Наиболее частые несерьезные нежелательные явления, возникающие как минимум у 5 % пациентов, включали снижение скорости клубочковой фильтрации, снижение уровня гемоглобина, снижение количества лимфоцитов, дыхательную недостаточность, анемию, повышение температуры тела, гипергликемию, повышение уровня креатинина в крови и повышение уровня глюкозы в крови (таблица S20). Частота этих нежелательных явлений в группах ремдесивира и плацебо в целом была одинаковой.
Кроссовер
Комиссия по мониторингу данных и безопасности рекомендовала предоставить спонсору предварительный отчет о первичном анализе. После этого данные о 51 пациенте (4,8 % от общего числа пациентов, включенных в исследование) — 16 (3,0 %) пациентов из группы ремдесивира и 35 (6,7 %) пациентов из группы плацебо — были демаскированы. 26 пациентов (74,3 %) из группы плацебо, чьи данные были демаскированы, получали ремдесивир. Анализы чувствительности, оценивающие демаскирование (данные пациентов, чье распределение в группы лечения было раскрыто, цензурировались по дате демаскирования) и кроссовер (данные пациентов из группы плацебо, получавших ремдесивир, были цензурированы по дате начала терапии ремдесивиром), дали результаты, аналогичные результатам первичного анализа (таблица S9).
Обсуждение
Это двойное слепое рандомизированное плацебо-контролируемое исследование продемонстрировало преимущества противовирусной терапии при COVID‑19. Общие результаты соответствовали данным предварительного отчета: 10-дневный курс ремдесивира превосходил плацебо при лечении госпитализированных пациентов с COVID‑19. У пациентов, получавших ремдесивир, выздоровление наступало быстрее, чем в группе плацебо (первичная конечная точка): медиана времени до выздоровления составила 10 дней в группе ремдесивира и 15 дней в группе плацебо; отношение частот выздоровления 1,29 (95 % ДИ 1,12–1,49). Шансы на улучшение категории по шкале клинического состояния на 15-й день в группе ремдесивира были выше (основная вторичная конечная точка; отношение шансов 1,5; 95 % ДИ 1,2–1,9). Данные по ряду дополнительных вторичных конечных точек в группе ремдесивира подтверждают эти результаты: более быстрое улучшение на 1-2 категории по шкале клинического состояния; меньшее время до выписки или до достижения целевых баллов (≤ 2) по шкале NEWS; более короткая средняя продолжительность первоначальной госпитализации (12 дней против 17 дней). Смертность от всех причин составила 11,4 % в группе ремдесивира и 15,2 % в группе плацебо (отношение рисков 0,73; 95 % ДИ 0,52–1,03).
Наши данные позволяют предположить, что терапия ремдесивиром может предотвратить прогрессирование заболевания и более тяжелое поражение дыхательной системы. Об этом свидетельствуют более низкая доля серьезных нежелательных явлений, обусловленных дыхательной недостаточностью, в группе ремдесивира, а также тот факт, что пациентам из группы ремдесивира, которые на момент включения в исследование не получали кислородотерапию, в ходе исследования кислородотерапия требовалась реже. Доля пациентов, нуждавшихся во время исследования в более высоком уровне респираторной поддержки, в группе ремдесивира также была ниже. Терапия ремдесивиром была связана с уменьшением продолжительности непрерывной кислородотерапии (среди пациентов, получавших кислородотерапию на момент включения в исследование). Кроме того, уменьшалась непрерывная продолжительность ИВЛ или ЭКМО среди пациентов, которые находились на ИВЛ или ЭКМО при включении в исследование. Таким образом, можно предположить, что терапия ремдесивиром не только облегчает течение болезни, но и позволяет более эффективно использовать ресурсы, ограниченные во время пандемии. Преимущества ремдесивира (оцененные по показателям выздоровления) сохранялись и после поправки на применение глюкокортикоидов. Это позволяет предположить, что положительные эффекты дексаметазона, продемонстрированные в исследовании RECOVERY [4], суммируются с положительными эффектами ремдесивира.
Преимущества ремдесивира были наиболее выраженными у пациентов с исходной категорией 5 по шкале клинического состояния (пациенты, получавшие низкопоточную кислородотерапию). Отчасти это различие может быть связано с большим размером выборки в этой категории; доверительные интервалы для исходно категории 4 (отсутствие кислородотерапии), 6 (высокопоточная кислородотерапия) и 7 (ЭКМО или ИВЛ) были широкими. Однако статистический анализ свидетельствует о более выраженных преимуществах ремдесивира (оцененных по показателям выздоровления и смертности) при низких категориях по шкале клинического состояния. При этом не следует считать, что при высоких категориях по шкале клинического состояния ремдесивир неэффективен. Среднее время выздоровления в категории 7 оценить невозможно; вероятно, период наблюдения в данном исследовании слишком короткий для данной подгруппы пациентов.
Наши результаты следует сравнить с результатами других рандомизированных клинических исследований по изучению применения ремдесивира. В китайское исследование Wang et al. в начале пандемии было включено 237 пациентов (158 получали ремдесивир, 79 — плацебо). Улучшение в группе ремдесивира наступало быстрее, чем в группе плацебо: через 21,0 день (95 % ДИ 13,0–28,0) и 23,0 дня (95 % ДИ 15,0–28,0), соответственно; отношение рисков для клинического улучшения 1,23; 95 % ДИ 0,87–1,75 [14]. Из-за локального контроля вспышки COVID‑19 набор в исследование завершили досрочно. Мощность этого исследования была ниже, чем мощность исследования ACTT-1, из-за меньшего размера выборки и рандомизации в соотношении 2:1. Кроме того, в китайском исследовании не были продемонстрированы какие-либо статистически значимые клинические преимущества ремдесивира.
Недавно было опубликовано открытое рандомизированное исследование по изучению применения ремдесивира у госпитализированных пациентов с COVID‑19 средней степени тяжести (83 % исходно не получали кислород). Пациенты, получавшие ремдесивир в течение 5 дней, имели более высокие шансы на клиническое улучшение, чем те, кто получал стандартную терапию (отношение шансов 1,65; 95 % ДИ 1,09–2,48; p = 0,02). При 10-дневном курсе ремдесивира этого преимущества не наблюдалось (p = 0,18) [15]. Мы считаем, что перечисленные исследования подтверждают наши выводы относительно эффективности ремдесивира. При этом данное исследование было более крупным, со слепым дизайном, и набор в исследование был полностью завершен.
На ранней стадии исследования первичная конечная точка была изменена. Исходно первичной конечной точкой было изменение категории по шкале клинического состояния на 15-й день, но ее заменили на время до выздоровления до 29-го дня. В феврале 2020 года, когда разрабатывался дизайн этого исследования, о клиническом течении COVID‑19 было известно немного. Согласно новым данным, COVID‑19 имеет более длительное течение, чем предполагалось ранее, и это вызвало опасения, что оценка состояния на 15-й день не выявит возможные различия в исходе после 15-го дня. Предложение об изменении первичной конечной точки внесли 22 марта 2020 г. статистики исследования; они не знали о распределении в группы лечения и не имели данных об исходах. Когда было предложено это изменение, в исследование было включено 72 пациента. Изменение первичной конечной точки не характерно для исследований, посвященных хорошо изученным заболеваниям. Однако признается, что в исследованиях, посвященных малоизученным болезням, могут возникнуть обстоятельства, требующие изменить способ оценки конечной точки или же заменить саму конечную точку [16]. В данном исследовании исходная первичная конечная точка стала основной вторичной конечной точкой. В итоге результаты как для первичной, так и для основной вторичной конечных точек статистически значимо различались между группами ремдесивира и плацебо.
В ходе клинического исследования возник ряд проблем. Исследование проводилось в то время, когда поездки и доступ в больницы были ограничены. Обучение, инициирующие и мониторинговые визиты часто проводились удаленно. Исследовательскому персоналу поручали дополнительные клинические обязанности, а болезни персонала истощали ресурсы. Во многих центрах не было необходимых средств индивидуальной защиты и материалов, необходимых для проведения исследования (например, тампоны для взятия мазков). Однако исследователи были заинтересованы в поиске нестандартных решений и преодолении этих проблем. Пациенты, включенные в исследование, отражали характеристики общей популяции, инфицированной SARS‑CoV‑2 в течение этого периода, и, соответственно, составили репрезентативную выборку.
Учитывая предварительные данные об эффективности ремдесивира, FDA (Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США) выдало экстренное разрешение на его применение. Этот документ, выданный 1 мая 2020 г. (изменен 28 августа 2020 г.), разрешал применять ремдесивир для лечения взрослых и детей, госпитализированных с подозрением на COVID‑19 или с лабораторно подтвержденным COVID‑19. С тех пор ремдесивир получил полное или условное одобрение в нескольких других странах. Однако смертность даже при применении ремдесивира остается высокой, и очевидно, что для многих пациентов терапии одним противовирусным препаратом будет недостаточно. В настоящее время изучается применение ремдесивира в сочетании с препаратами, модифицирующими иммунный ответ (например, барицитинибом, ингибитором янус-киназ, в исследовании ACTT‑2, и интерфероном бета-1a в исследовании ACTT‑3). Для дальнейшего улучшения исходов у пациентов с COVID‑19 необходим комплексный подход, включающий новые противовирусные препараты, модификаторы иммунного ответа или других внутренних путей, а также комбинированная терапия.
Литература
- Helmy YA, Fawzy M, Elaswad A, Sobieh A, Kenney SP, Shehata AA. The COVID-19 pandemic: a comprehensive review of taxonomy, genetics, epidemiology, diagnosis, treatment, and control. J Clin Med 2020;9(4):E1225-E1225. doi.org
- Cao B, Wang Y, Wen D, et al. A trial of lopinavir–ritonavir in adults hospitalized with severe Covid-19. N Engl J Med 2020;382:1787-1799. doi.org
- Borba MGS, Val FFA, Sampaio VS, et al. Effect of high vs low doses of chloroquine diphosphate as adjunctive therapy for patients hospitalized with severe acute respiratory syndrome coronavirus 2 (SARS-CoV-2) infection: a randomized clinical trial. JAMA Netw Open 2020;3(4):e208857-e208857. doi.org
- The RECOVERY Collaborative Group. Dexamethasone in hospitalized patients with Covid-19 — preliminary report. N Engl J Med. DOI: 10.1056/NEJMoa2021436. doi.org
- Sheahan TP, Sims AC, Leist SR, et al. Comparative therapeutic efficacy of remdesivir and combination lopinavir, ritonavir, and interferon beta against MERS-CoV. Nat Commun 2020;11:222-222. doi.org
- Agostini ML, Andres EL, Sims AC, et al. Coronavirus susceptibility to the antiviral remdesivir (GS-5734) is mediated by the viral polymerase and the proofreading exoribonuclease. mBio 2018;9(2):e00221-18-e00221-18. doi.org
- Brown AJ, Won JJ, Graham RL, et al. Broad spectrum antiviral remdesivir inhibits human endemic and zoonotic deltacoronaviruses with a highly divergent RNA dependent RNA polymerase. Antiviral Res 2019;169:104541-104541. doi.org
- Sheahan TP, Sims AC, Graham RL, et al. Broad-spectrum antiviral GS-5734 inhibits both epidemic and zoonotic coronaviruses. Sci Transl Med 2017;9:eaal3653-eaal3653. doi.org
- Wang M, Cao R, Zhang L, et al. Remdesivir and chloroquine effectively inhibit the recently emerged novel coronavirus (2019-nCoV) in vitro. Cell Res 2020;30:269-271. doi.org
- de Wit E, Rasmussen AL, Falzarano D, et al. Middle East respiratory syndrome coronavirus (MERS-CoV) causes transient lower respiratory tract infection in rhesus macaques. Proc Natl Acad Sci U S A 2013;110:16598-16603. doi.org
- de Wit E, Feldmann F, Cronin J, et al. Prophylactic and therapeutic remdesivir (GS-5734) treatment in the rhesus macaque model of MERS-CoV infection. Proc Natl Acad Sci U S A 2020;117:6771-6776. doi.org
- Royal College of Physicians. National Early Warning Score (NEWS) 2. 2017 rcplondon.ac.uk
- King JC, Beigel JH, Ison MG, et al. Clinical development of therapeutic agents for hospitalized patients with influenza: challenges and innovations. Open Forum Infect Dis 2019;6:ofz137-ofz137. doi.org
- Wang Y, Zhang D, Du G, et al. Remdesivir in adults with severe COVID-19: a randomised, double-blind, placebo-controlled, multicentre trial. Lancet 2020;395:1569-1578.doi.org
- Spinner CD, Gottlieb RL, Criner GJ, et al. Effect of remdesivir vs standard care on clinical status at 11 days in patients with moderate COVID-19: a randomized clinical trial. JAMA 2020;324:1048-1057. doi.org
- The CONSORT Group. 3b. Changes to trial design consort-statement.org