Пренатальная диагностика и медицина плода во время пандемии COVID-19: руководство IFMSS

Оригинал: Karger
Авторы: Jan Deprest et al. (от имени International Fetal Medicine and Surgery Society)
Опубликовано: 6 мая 2020, Fetal Diagnosis and Therapy
Перевод: Елена Алексеенкова, Наталья Карпова, Фонд профилактики рака
Краткое изложение
Пандемия COVID-19 стала серьезным испытанием как для пациентов, так и для системы здравоохранения, и бросила вызов устоявшимся практикам оказания медицинской помощи беременным женщинам, в том числе, проведения пренатальной диагностики и лечения внутриутробного плода. Целью издания данного документа являлось проведение обзора актуальной информации для оптимизации оказания пренатальной помощи. Приведено обсуждение возможных тактик ведения беременности и проведения внутриутробных вмешательств при пороках и аномалиях развития плода во время беременности на фоне как отрицательного, так и положительного результата исследования на SARS-CoV-2. Возможность применения большинства методов лечения плода имеет время-зависимый характер и не может быть отложено. В отсутствие дефицита ресурсов и персонала следует предлагать проведение манипуляций с доказанной эффективностью, с учетом всех рисков для плода и матери, а также для медицинских работников. На сегодняшний день данных о возможности вертикальной передачи инфекции недостаточно, но теоретически ее вероятность может возрастать при проведении некоторых манипуляций. Обследование беременной на коронавирусную инфекцию перед операцией позволит избежать или отложить определенные процедуры, если та является источником инфекции, а также надлежащим образом защитить медицинских работников. Лечение некоторых врожденных заболеваний может проводиться после родов. Консультирование по поводу фетальных вмешательств, которые могут повысить интра- или послеоперационную заболеваемость, должно проводиться с учетом доступности необходимых ресурсов. Методы лечения с недоказанной эффективностью предлагать не следует. Мы поддерживаем включение женщин в регистры и исследования, которые могут помочь понять воздействие COVID-19 на состояние беременной, внутриутробного плода и новорожденного.
Пренатальная диагностика и скрининг в эпоху COVID-19
Уже опубликован ряд руководств по особенностям ведения беременности и родов в эпоху COVID-19 [1–10]. Посещения медицинского учреждения во время беременности могут быть разнесены по времени [10], и, по возможности, должны применяться телемедицинские технологии [11] и оказание медицинской помощи на дому [6][7][10]. Первая консультация во время беременности может быть проведена дистанционно, по результатам домашнего теста на беременность. Цель первой консультации – выявление факторов риска, проявляющихся в первом триместре. Консультирование по поводу скрининга синдрома Дауна и получение согласия могут быть проведены виртуально. УЗИ при сроке 12–13 недель может быть использовано для определения сроков беременности, жизнеспособности плода, количества плодов и хорионов, исключения значимых структурных аномалий и определения толщины воротникового пространства плода. Посещение медицинского учреждения для проведения УЗИ предпочтительно совместить с взятием крови для проведения рутинных исследований, а также биохимического или неинвазивного пренатального скрининга. Последующие консультации для обсуждения результатов исследований могут быть виртуальными. УЗИ с целью оценки анатомических структур следует отложить до срока 20–22 недели, когда его результаты будут более точными.
Ведение беременности у женщин с инфекцией, вызванной SARS-CoV-2
По-видимому, беременные женщины не являются более склонными к развитию COVID-19 и тяжелой степени его течения. До 9% случаев COVID-19 на фоне беременности могут сопровождаться тяжелым течением, но более, чем у 90% пациенток течение легкое [12][13][14][15][16][17].
- Для бессимптомных пациенток или при малой выраженности симптомов COVID-19 большинство скринингов плода можно безопасно отложить до выздоровления. Если пропущено временное окно для скрининга на трисомию 21, его рациональной альтернативой является неинвазивный пренатальный скрининг.
- Инфекция SARS-CoV-2 во время беременности может увеличивать риск преждевременных родов или задержки роста плода [4], поэтому некоторые врачи рекомендуют проводить УЗИ-мониторинг с интервалом в 4 недели для определения темпов роста, объема околоплодных вод и проведения допплерографии кровотока в пупочной артерии [2][4].
- У симптомных беременных необходимо оценивать состояние плода, так как дыхательная недостаточность матери может привести к дистрессу плода. По возможности, роды следует вести через естественные родовые пути. Относительно назначения глюкокортикоидов (ГКС) с целью созревания легких плода при инфекции COVID-19 обсуждаются потенциально возможные побочные эффекты. Данные о них частично основываются на наблюдениях, согласно которым ГКС усиливают репликацию вируса при определенных обстоятельствах [23]. По этой причине ГКС не следует назначать SARS-CoV-2-положительным пациенткам без или со слабовыраженными симптомами, кроме случаев угрожающих преждевременных родов до 34+0 недель [2][24]. Решение о назначении ГКС пациенткам, находящимся в интенсивной терапии, а также при сроке более 34+0 недель гестации, должно быть тщательно взвешено.
В настоящее время свидетельств спонтанной вертикальной передачи SARS-CoV-2 мало, что является несколько контринтуитивным, если учитывать высокую экспрессию его рецептора – ангиотензинпревращающего фермента 2 – в плаценте [26][27]. Одно из возможных объяснений заключается в том, что в плаценте не экспрессируется трансмембранная сериновая протеаза TMPRSS2, которая также играет роль в процессе проникновения вируса SARS-CoV-2 в клетку, – однако это лишь гипотеза [28][29].
Сообщений об обнаружении вируса в околоплодных водах или пуповинной крови (пока) нет [13]. Еще слишком рано утверждать, является ли спонтанная передача вируса при ранних сроках беременности более вероятной и/или имеет ли она более неблагоприятные последствия, но регистры исходов беременности при COVID-19 должны помочь это прояснить. Антитела IgM были обнаружены в сыворотке крови вскоре после рождения у трех новорожденных с симптомами заболевания [32][33], что свидетельствует в пользу внутриутробного вирусного воздействия, но исследование на основе IgM может быть ложно положительным [34].
Медицина плода в период пандемии COVID-19
Большинство манипуляций, связанных с медициной плода, являются время-зависимыми, и их отсрочка может ухудшить исходы для плода, новорожденного и даже матери [35][36][37][38].
Любая инвазивная процедура у SARS-CoV-2-положительной женщины теоретически является опасной в отношении вертикальной передачи инфекции.
Нет никаких доказательств того, что такая вертикальная передача возможна для COVID-19, поэтому следует продолжать предлагать минимально инвазивные процедуры (например, амниоцентез или фетоскопию). В идеале следует избегать трансплацентарного доступа, который увеличивает риск внутриамниотического кровотечения и нарушает фето-плацентарный барьер. Таким образом, амниоцентез может быть предпочтительнее биопсии ворсин хориона (Таблица 1).
Для беременных с симптомным течением COVID-19 предпочтительно по возможности отложить внутриутробные вмешательства.
Вмешательства, направленные на сохранение жизни плода
Следует продолжать проведение жизненно необходимых вмешательств, которые выполняются в условиях местной анестезии и седации [41], в их числе – фетоскопическая лазерная абляция плацентарных анастомозов при синдроме фето-фетальной трансфузии (СФФТ). Также следует продолжать проведение переливания крови и шунтирования при водянке плода, связанной с кистозно-аденоматозной мальформацией легкого (Таблица 1). Не следует продолжать проведение инвазивных исследований или вмешательств с недоказанной эффективностью.
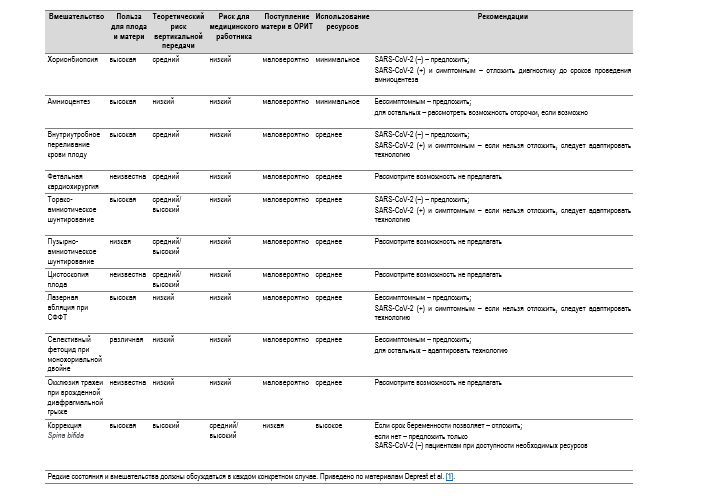
Таблица 1. Диагностические и терапевтические вмешательства, оценка рисков и пользы, а также точка зрения, основанная на текущих данных и доступных ресурсах
Обследование на SARS-CoV-2 перед внутриутробным вмешательством
Зачем проводить скрининг?
При положительном результате исследования может потребоваться изоляция пациентки, отсрочка или отмена проведения вмешательства и/или обязательное использование медицинскими работниками средств индивидуальной защиты (СИЗ).
У всех бессимптомных пациентов, которые перенесли крупную плановую операцию под общей анестезией во время инкубационного периода COVID-19, что было установлено ретроспективно, развилась пневмония; 44% были госпитализированы в ОРИТ и 20% умерли от острого респираторного дистресс-синдрома [40]. Средний возраст в выборке (55 лет, диапазон 21–84 года) не репрезентативен для беременных женщин, но хирургическое вмешательство при общей анестезии во время инкубационного периода инфекции представляет более высокий риск прогрессирования заболевания и осложнений, чем в сопоставимых контрольных группах [43]. Для пациентов, которые перенесли хирургическое вмешательство меньшего объема (в том числе, кесарево сечение), риск был ниже (8%), но все же значительно выше нормы [40].
Выявление и изоляция SARS-CoV-2-положительных пациентов также предотвращает появление в медицинских учреждениях «суперспредеров» (суперраспространителей), которые потенциально могут инфицировать многих пациентов и медицинских работников [44], особенно если они проходят процедуры с генерацией аэрозолей. Наконец, существует теоретический риск вертикальной передачи инфекции во время операции у активно выделяющих вирус пациенток.
Как проводить скрининг?
- анкетирование на наличие симптомов;
- взятие мазка из носоглотки и исследование методом RT-PCR на РНК SARS-CoV-2 – золотой стандарт диагностики;
- исследование крови на IgM и IgG к SARS-CoV-2.
Кому проводить скрининг?
Исходя из современных данных, представляется логичным проводить обследование всех пациентов, поступающих в стационар (включая женщин, у которых планируются внутриутробные вмешательства).
Послеродовое обследование новорожденного с врожденными аномалиями/пороками развития во время пандемии COVID-19
Если у матери положительный результат исследования на SARS-CoV-2, новорожденные должны быть проверены через 24 ч после рождения. RT-PCR является золотым стандартом, и достоверным подтверждением инфекции считается положительный результат исследования методом RT-PCR носо-/ротоглоточного или ректального мазка [51].
Аспекты интенсивной терапии новорожденного, находившегося в контакте с больным COVID-19
На сегодняшний день нет сообщений о новорожденных с врожденными аномалиями развития и сопутствующей инфекцией COVID-19. Неонатальные рентгенографические критерии еще не установлены.
Новорожденные в ОРИТН в идеале должны находиться в кувезе в помещении с отрицательным давлением. Рекомендуется соблюдать меры предосторожности в отношении контактной и воздушно-капельной передачи инфекции, кроме случаев, когда новорожденный подвергается аэрозоль-генерирующим процедурам (например, санация дыхательных путей, неинвазивная вентиляция легких, в т.ч. с непрерывным положительным давлением в дыхательных путях, интубация/экстубация или механическая вентиляция легких) и становится необходимым соблюдение мер в отношении аэрозольной передачи и ношение полного комплекта СИЗ. С учетом распространенности использования у новорожденных трубок без манжеты, как обычная, так и высокочастотная вентиляция легких связана с некоторым риском образования аэрозолей.
Бессимптомная пациентка может инфицировать новорожденного во время ухода или грудного вскармливания. Рутинное ношение лицевой маски матерью и соблюдение мер гигиены могут снизить риск инфицирования.
Лечение новорожденных с врожденными аномалиями или патологическими состояниями должно продолжаться насколько позволяют ресурсы. По возможности, хирургическое вмешательство следует отложить до тех пор, пока результаты исследования на COVID-19 не будут отрицательными.
Краткосрочные исходы у новорожденных, положительных на SARS-CoV-2, представляются благоприятными, причем у большинства из них наблюдаются только легкие симптомы. До сих пор среди новорожденных не было зарегистрировано случаев тяжелой коронавирусной пневмонии или смерти в результате этой болезни [13][31][33][55][56][57]. Симптомы одного новорожденного в тяжелом состоянии были связаны, вероятно, с недоношенностью и с бактериальной, а не вирусной инфекцией [33].
Нет никаких доказательств того, что иммуноглобулины, противовирусные препараты или стероиды улучшают результаты лечения.
Использование ресурсов
Возможно, логичным является приостановление вмешательств повышенной сложности в сфере фетальной хирургии ввиду необходимости привлечения для них дополнительного медицинского персонала, потенциальной потребности в койках интенсивной терапии и/или длительности пребывания в стационаре [41]. В отличие от них, жизненно необходимые переливания крови плоду и фетоскопическая лазерная коагуляция при СФФТ часто могут быть выполнены в амбулаторных условиях или требуют кратковременной госпитализации.
Заключение
COVID-19 оказывает огромное давление на пациентов, медицинских работников и систему здравоохранения. Тем не менее, необходимо поддерживать медицину плода и оказание медицинской помощи беременным женщинам, и мы должны стремиться защитить уязвимую популяцию беременных женщин и их детей. Наши рекомендации кратко изложены в Таблице 2. Они касаются как SARS-CoV-2-отрицательных, так и SARS-CoV-2-положительных пациенток с аномалиями и пороками развития плода, для которых проведение внутриутробного вмешательства может нести пользу. При мультидисциплинарном обсуждении отдельных случаев следует задействовать все доступные ресурсы. Медицинский персонал должен обсудить с родителями риски и преимущества любой процедуры, включая возможность хирургических осложнений. В конечном счете, принимаемые решения будут зависеть от состояния плода и матери, а также от текущей местной обстановки.
Таблица 2. Краткое изложение рекомендаций
- Рутинная медицинская помощь беременным женщинам должна быть скорректирована с использованием дополнительных временных интервалов между посещениями пациенток, телемедицины и методов оказания помощи на дому. Проведение УЗ- и неинвазивного пренатального скрининга также может потребовать корректировки.
- Если позволяют ресурсы, возможно, найдется место для проведения всеобщего тестирования беременных женщин на наличие инфекции SARS-CoV-2. Мы настоятельно рекомендуем проводить тестирование перед любым оперативным вмешательством.
- Заболевание, связанное с SARS-CoV-2, может протекать у беременных женщин с различной степенью тяжести. Неясно, являются ли они более восприимчивыми к SARS-CoV-2. Тактика ведения пациентки должна определяться тяжестью течения заболевания и характером осложнений. Кесарево сечение следует проводить по обычным акушерским показаниям и рассматривать в случаях септического шока или острой органной недостаточности. Роды также могут облегчить вентиляцию легких у матери.
- В настоящее время имеются недостаточные и неподтвержденные данные о спонтанной вертикальной передаче SARS-CoV-2. Теоретически этот риск может увеличиваться при проведении внутриутробных вмешательств при повреждении фето-плацентарного барьера или кожи плода. Следует избегать трансплацентарного доступа.
- Вмешательства, относящиеся к медицине плода, носят время-зависимый характер, поэтому не должны рассматриваться как плановые. У пациентов с SARS-CoV-2 можно рассмотреть возможность отсрочки вмешательства, чтобы избежать хирургических осложнений, при условии, что процедура может быть отложена. Особенно это касается сложных процедур, требующих использования общей анестезии, и вмешательств у симптомных пациенток. И, наоборот, проведение жизненно необходимых малоинвазивных вмешательств должно продолжаться.
- Не следует предлагать процедуры с недоказанной эффективностью.
- При уходе за новорожденным, у матери которого подозрение или подтвержденный COVID-19, должны применяться строгие меры контроля за распространением инфекции, в том числе, карантин. На основании имеющихся данных, у новорожденных обычно наблюдается легкое течение инфекции COVID-19, и краткосрочные исходы для них благоприятные.
- Медицинские работники подвергаются значительному риску инфицирования SARS-CoV-2, что является аргументом в пользу тестирования пациентов. При уходе за больными с подозрением или подтвержденным SARS-CoV-2 всегда следует использовать соответствующие средства индивидуальной защиты.
- Пандемия COVID-19 поражает мир неравномерно. Центры должны периодически пересматривать и корректировать свой подход к медицине плода по мере изменения потребностей и имеющихся ресурсов.
- При согласии женщин с SARS-CoV-2 на проведение внутриутробных вмешательств с доказанной эффективностью нет этического обязательства предоставлять информацию о теоретических рисках. Информированное согласие предоставляет информацию о разумных вариантах, их преимуществах и рисках, а также поддерживает понимание и оценку пациентом своих собственных ценностей и убеждений.
- Возможность прерывания беременности зависит от времени, и его проведение не должно рассматриваться как «не экстренное».
- Рекомендуется документировать исходы для матери и плода, потому что данные о большой когорте пациентов быстро приумножат наши знания.
Список литературы:
- Deprest J, Van Ranst M, Lannoo L, Bredaki E, Ryan G, David A, et al. Feto-placental surgeries during the covid-19 pandemic: starting the discussion. Prenat Diagn. 2020. doi: 10.1002/pd.5702.
- Favre G, Pomar L, Qi X, Nielsen-Saines K, Musso D, Baud D. Guidelines for pregnant women with suspected SARS-CoV-2 infection. Lancet Infect Dis. 2020 Mar;S1473-3099(20)30157-2.
- Bahtiyar MO, Baschat A, Deprest J, Emery S, Goodnight W, Johnson A, McCullough L, Moldenhauer J, Ryan G, Tsao KB, Van Mieghem T, Wagner A, Zaretsky Z. Fetal interventions in the setting of COVID-19 pandemic: statement from the North American Fetal Therapy Network (NAFTNet). Am J Obstet Gynecol. 2020. doi: 10.1016/j.ajog.2020.04.025.
- Dashraath P, Wong JL, Lim MX, Lim LM, Li S, Biswas A, et al. Coronavirus disease 2019 (COVID-19) pandemic and pregnancy. Am J Obstet Gynecol. 2020 Mar;S0002-9378(20)30343-4.
- NHS. Specialty guides: coronavirus. 2020. Available from: england.nhs.uk.
- Abu-Rustum RS, Sotiriadis A, et al. ISUOG consensus statement on organization of routine and specialist obstetric ultrasound services in the context of COVID‐19. Ultra Obstet Gynecol. 2020. doi: 10.1002/uog.22029.
- Boelig RC, Bellussi F, Berghella V. MFM Guidance for COVID-19. Am J Obstet Gynecol. Forthcoming 2020.
- Chen D, Yang H, Cao Y, Cheng W, Duan T, Fan C, et al. Expert consensus for managing pregnant women and neonates born to mothers with suspected or confirmed novel coronavirus (COVID-19) infection. Int J Gynaecol Obstet. 2020 May;149(2):130–6.
- Chen Y, Li Z, Zhang YY, Zhao WH, Yu ZY. Maternal health care management during the outbreak of coronavirus disease 2019. J Med Virol. 2020 Mar;jmv.25787.
- Poon LC, Yang H, Lee JC, Copel JA, Leung TY, Zhang Y, et al. ISUOG Interim Guidance on 2019 novel coronavirus infection during pregnancy and puerperium: information for healthcare professionals. Ultrasound Obstet Gynecol. 2020 Mar;uog.22013.
- Hollander JE, Carr BG. Virtually Perfect? Telemedicine for Covid-19. N Engl J Med. 2020 Mar;NEJMp2003539.
- World Health Organization. Report of the WHO-China joint mission on coronavirus disease 2019 (COVID-19). Geneva: WHO; 2020.
- Chen H, Guo J, Wang C, Luo F, Yu X, Zhang W, et al. Clinical characteristics and intrauterine vertical transmission potential of COVID-19 infection in nine pregnant women: a retrospective review of medical records. Lancet. 2020 Mar;395(10226):809–15.
- Huang C, Wang Y, Li X, Ren L, Zhao J, Hu Y, et al. Clinical features of patients infected with 2019 novel coronavirus in Wuhan, China. Lancet. 2020 Feb;395(10223):497–506.
- Liu H, Liu F, Li J, Zhang T, Wang D, Lan W. Clinical and CT imaging features of the COVID-19 pneumonia: focus on pregnant women and children. J Infect. 2020 May;80(5):e7–13.
- Qiao J. What are the risks of COVID-19 infection in pregnant women? Lancet. 2020 Mar;395(10226):760–2.
- Rasmussen SA, Smulian JC, Lednicky JA, Wen TS, Jamieson DJ. Coronavirus Disease 2019 (COVID-19) and pregnancy: what obstetricians need to know. Am J Obstet Gynecol. 2020 Feb;222(5):S0002-9378(20)30197-6.
- Ashokka B, Loh MH, Tan CH, Su LL, Young BE, Lye DC, et al. Care of the Pregnant Woman with COVID-19 in Labor and Delivery: Anesthesia, Emergency cesarean delivery, Differential diagnosis in the acutely ill parturient, Care of the newborn, and Protection of the healthcare personnel. Am J Obstet Gynecol. 2020 Apr;S0002-9378(20)30430-0.
- Rothe C, Schunk M, Sothmann P, Bretzel G, Froeschl G, Wallrauch C, et al. Transmission of 2019-nCoV Infection from an Asymptomatic Contact in Germany. N Engl J Med. 2020 Mar;382(10):970–1.
- Wei WE, Li Z, Chiew CJ, Yong SE, Toh MP, Lee VJ. Presymptomatic Transmission of SARS-CoV-2 - Singapore, January 23-March 16, 2020. MMWR Morb Mortal Wkly Rep. 2020 Apr;69(14):411–5.
- Wang W, Xu Y, Gao R, Lu R, Han K, Wu G, et al. Detection of SARS-CoV-2 in Different Types of Clinical Specimens. JAMA. 2020. doi: 10.1001/jama.2020.3786.
- Zhou F, Yu T, Du R, Fan G, Liu Y, Liu Z, et al. Clinical course and risk factors for mortality of adult inpatients with COVID-19 in Wuhan, China: a retrospective cohort study. Lancet. 2020 Mar;395(10229):1054–62.
- Van Damme E, Sauviller S, Lau B, Kesteleyn B, Griffiths P, Burroughs A, et al. Glucocorticosteroids trigger reactivation of human cytomegalovirus from latently infected myeloid cells and increase the risk for HCMV infection in D+R+ liver transplant patients. J Gen Virol. 2015 Jan;96(Pt 1):131–43.
- ObGproject. COVID-19: the SMFM/SOAP guidelines for labor and delivery. 2020. Available from: obgproject.com.
- Melamed N, Asztalos E, Murphy K, Zaltz A, Redelmeier D, Shah BR, et al. Neurodevelopmental disorders among term infants exposed to antenatal corticosteroids during pregnancy: a population-based study. BMJ Open. 2019 Sep;9(9):e031197.
- Levy A, Yagil Y, Bursztyn M, Barkalifa R, Scharf S, Yagil C. ACE2 expression and activity are enhanced during pregnancy. Am J Physiol Regul Integr Comp Physiol. 2008 Dec;295(6):R1953–61.
- Zhou P, Yang XL, Wang XG, Hu B, Zhang L, Zhang W, et al. A pneumonia outbreak associated with a new coronavirus of probable bat origin. Nature. 2020 Mar;579(7798):270–3.
- Hoffmann M, Kleine-Weber H, Schroeder S, Kruger N, Herrler T, Erichsen S, et al. SARS-CoV-2 cell entry depends on ACE2 and TMPRSS2 and is blocked by a clinically proven protease inhibitor. Cell. 2020 Apr 16;181(2):271-80 e8.
- The Human Protein Atlas. TMPRSS2. Available from: proteinatlas.org, accessed April 19th 2020.
- Fan C, Lei D, Fang C, Li C, Wang M, Liu Y, et al. Perinatal Transmission of COVID-19 Associated SARS-CoV-2: Should We Worry? Clin Infect Dis. 2020 Mar;ciaa226.
- Zhu H, Wang L, Fang C, Peng S, Zhang L, Chang G, et al. Clinical analysis of 10 neonates born to mothers with 2019-nCoV pneumonia. Transl Pediatr. 2020 Feb;9(1):51–60.
- Dong L, Tian J, He S, Zhu C, Wang J, Liu C, et al. Possible Vertical Transmission of SARS-CoV-2 From an Infected Mother to Her Newborn. JAMA. 2020. doi: 10.1001/jama.2020.4621.
- Zeng L, Xia S, Yuan W, Yan K, Xiao F, Shao J, et al. Neonatal early-onset infection with SARS-CoV-2 in 33 neonates born to mothers with COVID-19 in Wuhan, China. JAMA Pediatr. 2020. doi: 10.1001/jamapediatrics.2020.0878.
- Kimberlin DW, Stagno S. Can SARS-CoV-2 infection be acquired in utero? More definitive evidence is needed. JAMA. 2020. doi: 10.1001/jama.2020.4868.
- Braun T, Brauer M, Fuchs I, Czernik C, Dudenhausen JW, Henrich W, et al. Mirror syndrome: a systematic review of fetal associated conditions, maternal presentation and perinatal outcome. Fetal Diagn Ther. 2010;27(4):191–203.
- Chimenea A, García-Díaz L, Calderón AM, Heras MM, Antiñolo G. Resolution of maternal Mirror syndrome after succesful fetal intrauterine therapy: a case series. BMC Pregnancy Childbirth. 2018 Apr;18(1):85.
- American College of Obstetricians and Gynecologists. Joint statement on abortion access during the COVID-19 outbreak 2020. 2020. Available from: acog.org.
- SMFM. Joint statement on elective surgeries. 2020. Available from: s3.amazonaws.com.
- Zhang L, Jiang Y, Wei M, Cheng BH, Zhou XC, Li J, et al. [Analysis of the pregnancy outcomes in pregnant women with COVID-19 in Hubei Province]. Zhonghua Fu Chan Ke Za Zhi. 2020 Mar;55(0):E009.
- Lei S, Jiang F, Su W, Chen C, Chen J, Mei W, et al. Clinical characteristics and outcomes of patients undergoing surgeries during the incubation period of COVID-19 infection. EClinicalMedicine. 2020 Apr 5:100331.
- Sacco A, Van der Veeken L, Bagshaw E, Ferguson C, Van Mieghem T, David AL, et al. Maternal complications following open and fetoscopic fetal surgery: A systematic review and meta-analysis. Prenat Diagn. 2019 Mar;39(4):251–68.
- Peralta CF, Botelho RD, Romano ER, Imada V, Lamis F, Júnior RR, et al. Fetal open spinal dysraphism repair through a mini-hysterotomy: influence of gestational age at surgery on the perinatal outcomes and postnatal shunt rates. Prenat Diagn. 2020. doi: 10.1002/pd.5675.
- Wang D, Zhou M, Nie X, Qiu W, Yang M, Wang X, et al. Epidemiological characteristics and transmission model of Corona Virus Disease 2019 in China. J Infect. 2020 May;80(5):e25–7.
- Li YK, Peng S, Li LQ, Wang Q, Ping W, Zhang N, et al. Clinical and transmission characteristics of Covid-19: a retrospective study of 25 cases from a single thoracic surgery department. Curr Med Sci. 2020 Apr;40(2):295–300.
- Centers for Disease Control and Prevention. Symptoms of coronavirus. 2020. Available from: cdc.gov.
- Sutton D, Fuchs K, D’Alton M, Goffman D. Universal screening for SARS-CoV-2 in women admitted for delivery. N Engl J Med. 2020 Apr;NEJMc2009316.
- Wölfel R, Corman VM, Guggemos W, Seilmaier M, Zange S, Müller MA, et al. Virological assessment of hospitalized patients with COVID-2019. Nature. 2020. doi: 10.1038/s41586-020-2196-x.
- Iacobucci G. Covid-19: hospitals can remove 15% cap on testing of NHS staff. BMJ. 2020 Apr;369:m1339.
- To KK, Tsang OT, Leung WS, Tam AR, Wu TC, Lung DC, et al. Temporal profiles of viral load in posterior oropharyngeal saliva samples and serum antibody responses during infection by SARS-CoV-2: an observational cohort study. Lancet Infect Dis. 2020 Mar;S1473-3099(20)30196-1.
- Zhao J, Yuan Q, Wang H, Liu W, Liao X, Su Y, et al. Antibody responses to SARS-CoV-2 in patients of novel coronavirus disease 2019. Clin Infect Dis. 2020 Mar;ciaa344.
- Cook TM, El-Boghdadly K, McGuire B, McNarry AF, Patel A, Higgs A. Consensus guidelines for managing the airway in patients with COVID-19: Guidelines from the Difficult Airway Society, the Association of Anaesthetists the Intensive Care Society, the Faculty of Intensive Care Medicine and the Royal College of Anaesthetists. Anaesthesia. 2020. doi: 10.1111/anae.15054.
- Zhang J, Wang S, Xue Y. Fecal specimen diagnosis 2019 novel coronavirus-infected pneumonia. J Med Virol. 2020 Mar;92(6):680–2.
- Zhang W, Du RH, Li B, Zheng XS, Yang XL, Hu B, et al. Molecular and serological investigation of 2019-nCoV infected patients: implication of multiple shedding routes. Emerg Microbes Infect. 2020 Feb;9(1):386–9.
- Cascella M, Rajnik M, Cuomo A, Dulebohn SC, Di Napoli R. Features, Evaluation and Treatment Coronavirus (COVID-19). Treasure Island (FL): StatPearls; 2020.
- Lu Q, Shi Y. Coronavirus disease (COVID-19) and neonate: what neonatologist need to know. J Med Virol. 2020 Mar;92(6):564–7.
- Schwartz DA. An analysis of 38 pregnant women with COVID-19, their newborn infants, and maternal-fetal transmission of SARS-CoV-2: maternal coronavirus infections and pregnancy outcomes. Arch Pathol Lab Med. 2020. doi: 10.5858/arpa.2020-0901-SA.
- Yu N, Li W, Kang Q, Xiong Z, Wang S, Lin X, et al. Clinical features and obstetric and neonatal outcomes of pregnant patients with COVID-19 in Wuhan, China: a retrospective, single-centre, descriptive study. Lancet Infect Dis. 2020 Mar;S1473-3099(20)30176-6.
- Huang L, Lin G, Tang L, Yu L, Zhou Z. Special attention to nurses’ protection during the COVID-19 epidemic. Crit Care. 2020 Mar;24(1):120.
- Ling L, Joynt GM, Lipman J, Constantin JM, Joannes-Boyau O. COVID-19: A critical care perspective informed by lessons learnt from other viral epidemics. Anaesth Crit Care Pain Med. 2020 Feb;39(2):S2352-5568(20)30029-1.
- icmanaesthesiacovid-19.org, accessed 19 April 2020.
- David JB, Nicholas CC, Matthew JH, et al. Consensus statement: safe airway Society principles of airway management and tracheal intubation specific to the COVID-19 adult patient group. Med J Aust. 2020. Available from: mja.com.au.
- Centers for Disease Control and Prevention. Guidelines for environmental infection control in health-care facilities: Appendix B – Air. 2003. Available from: cdc.gov.
- McCullough LB, Chervenak FA. Professional Ethics in Obstetrics and Gynecology. Cambridge, New York: Cambridge University Press; 2020.
- Musso D, Ko AI, Baud D. Zika Virus Infection - After the Pandemic. N Engl J Med. 2019 Oct;381(15):1444–57.
- PRIORITY (Pregnancy CoRonavIrus Outcomes RegIsTrY). PRIORITY. 2020. Available from: priority.ucsf.edu.
- PAN COVID. An international registry of pregnancy and neonatal outcomes of COVID. 2020. Available from: pan-covid.yolasite.com.
- CHUV. COVI-Preg International COVID-19 and Pregnancy Registry. 2020. Available from: covi-preg.ch.
- Wellcome. Sharing research data and findings relevant to the novel coronavirus (COVID-19) outbreak. 2020. Available from: wellcome.ac.uk.