Повторная оценка эффективности противовирусных препаратов для лечения COVID-19, результаты промежуточных исследований ВОЗ

Оригинал: MedRxiv
Автор: WHO (ВОЗ) - WHO Solidarity trial consortium (Консорциум клинических испытаний ВОЗ): Nuffield Department of Population Health, University of Oxford, Oxford, et al.
Опубликовано: 15 октября 2020, MedRxiv
Перевод: Анна Селюта, ФГБУ НМИЦ онкологии им Н.Н. Петрова, Фонд “Не напрасно!”
Редакция: Наталья Рожкова, Фонд “Не напрасно!”
ПРИМЕЧАНИЕ. В этом препринте сообщается о новом исследовании, которое не было сертифицировано экспертной оценкой и не должно использоваться в качестве руководства для клинической практики.
Аннотация
Данные
Экспертные группы ВОЗ рекомендовали провести исследования смертности для 4 перепрофилированных противовирусных препаратов у госпитализированных пациентов с COVID-19.
Методы
Исследуемые препараты: Ремдесивир, Гидроксихлорохин, Лопинавир (комбинация фиксированных доз с Ритонавиром) и Интерферон-β1a (в основном подкожно; сначала в комбинации с Лопинавиром, затем - без него). Госпитализированные пациенты с COVID-19 были рандомизированы в равной степени между всеми исследуемыми доступными локально препаратами и контрольной группой (5 вариантов: 4 препарата и местная стандартная терапия). Первичный анализ лечения - это госпитальная смертность в 4-х сравнениях попарно каждого исследуемого препарата с его контролем (одновременно назначалось такое же лечение без этого препарата, несмотря на его доступность). 28-дневные риски Каплана-Мейера не стратифицированы; Логарифмические коэффициенты смертности (RR) стратифицированы по возрасту и необходимости в искусственной вентиляции легких (ИВЛ) при поступлении.
Результаты
В 405 больницах в 30 странах было рандомизированно 11 266 взрослых пациентов, 2750 из них получили ремдесивир, 954 гидроксихлорохин, 1411 лопинавир, 651 интерферон плюс лопинавир, 1412 только интерферон и 4088 местную стандартную терапию. Комплаентность составляла 94–96% в середине лечения с перекрестным переходом 2–6%. Сообщалось о 1253 случаях смерти (медиана 8-го дня, IQR 4–14). Смертность по Каплану-Мейеру за 28 дней составила 12% (39%, если ИВЛ уже проводилась при рандомизации, 10% в другом случае). Коэффициенты смертности (с 95%-м доверительным интервалом и числом умерших / рандомизированных, каждое лекарство по сравнению со своим контролем) составляли: RR ремдесивира = 0,95 (0,81-1,11, p = 0,50; 301/2743 препарат против 303/2708 контроля), RR гидроксихлорохина = 1,19 (0,89-1,59, p = 0,23; 104/947 против 84/906), RR лопинавира = 1,00 (0,79-1,25, p = 0,97; 148/1399 против 146/1372) и RR интерферона = 1,16 (0,96-1,39, p = 0,11; 243/2050 против 216/2050). Ни один исследуемый препарат не снизил смертность (ни у пациентов на ИВЛ ни у любой другой подгруппы), начало ИВЛ или продолжительность госпитализации.
Выводы
Схемы лечения с ремдесивиром, гидроксихлорохином, лопинавиром и интерфероном оказали незначительное влияние или не оказали никакого влияния на пациентов, госпитализированных с COVID-19, о чем свидетельствуют общая смертность, начало проведения ИВЛ и продолжительность пребывания в больнице. Данные о смертности содержат большую часть рандомизированных данных по ремдесивиру и интерферону и согласуются с метаанализами смертности во всех основных исследованиях. (Финансирование: ВОЗ. Регистрация: ISRCTN83971151, NCT04315948)
Введение
Исследовательский форум ВОЗ по COVID-19 в феврале 2020 года рекомендовал проводить оценку методов лечения в крупных рандомизированных испытаниях [1]. А другие группы экспертов ВОЗ определили 4 перепрофилированных противовирусных препарата, которые могут оказать как минимум умеренное влияние на смертность: ремдесивир, гидроксихлорохин, лопинавир и интерферон-β1a [2]. В марте 2020 года ВОЗ начала крупное простое открытое рандомизированное исследование с участием многих стран среди госпитализированных пациентов, посвященное изучению влияния этих 4 препаратов на смертность во время госпитализации. Испытание было адаптивным; бесперспективные препараты могут быть исключены, а другие добавлены. Гидроксихлорохин и лопинавир в конечном итоге были исключены, но будут добавлены другие, такие как моноклональные антитела. Мы сообщаем промежуточные результаты по смертности для 4 исходных препаратов.
Методы
Протокол [3] был разработан для участия сотен потенциально подверженных инфекции больниц в десятках стран. Поэтому заполнение формы не требовалось, а методика проведения исследования была минимальной, но строгой. Онлайн-рандомизация давших согласие пациентов (через облачную систему управления клиническими данными, совместимую с GCP (Good Clinical Practice - надлежащая клиническая практика;) заняла всего несколько минут, как и онлайн-сообщение о смерти в больнице или выписке (плюс краткие сведения о респираторной поддержке в больнице и использовании исследуемых препаратов и некоторых препаратов вне рамок исследования). Никаких других отчетов не требовалось, если только врачи не подозревали неожиданную серьезную побочную реакцию (SUSAR). Национальные и глобальные мониторы решали вопросы и проверяли прогресс и полноту указываемых данных. Подходящие для исследования пациенты были в возрасте ≥18 лет, госпитализированы с диагнозом COVID-19, не получали никаких исследуемых препаратов, без ожидаемого перевода в другое отделение в течение 72 часов и, по мнению врача, без противопоказаний к какому-либо исследуемому препарату. Участники были рандомизированы в равных пропорциях между контрольными препаратами и любыми другими исследуемыми препаратами, доступными на местном уровне (до 5 вариантов: эти препараты и местная стандартная терапия). Плацебо не использовались. Изучаемые препараты: ремдесивир, гидроксихлорохин, лопинавир-ритонавир и интерферон (вводился вместе с лопинавиром до 4 июля). Прием гидроксихлорохина и лопинавира был прекращен из-за отсутствия эффективности 18 июня и 4 июля 2020 г., соответственно; интерферон прекращается 16 октября.
Суточные дозы были теми, которые уже применялись при других заболеваниях, но чтобы увеличить эффективность без чрезмерного сердечного риска, доза гидроксихлорохина была основана на дозе для амебного абсцесса печени, а не на более низкой дозе как при малярии [4] . Гидроксихлорохин слегка удлиняет интервал QT и чрезмерно высокая доза или быстрое введение могла вызвать аритмию или гипотонию.
Все препараты были отменены при выписке.
Схемы были следующими:
- ремдесивир (внутривенный): 0 день, 200 мг; дни 1-9, 100 мг.
- гидроксихлорохин (перорально): 0 час - 4 таблетки; 6 час - 4 таблетки; 12 час - начать по 2 таблетки 2 раза в день в течение 10 дней. Каждая таблетка содержала 200 мг гидроксихлорохина сульфата (155 мг основного вещества на таблетку; малоиспользуемая альтернатива: хлорохин - 155 мг основного вещества на таблетку).
- лопинавир (перорально): 2 таблетки 2 раза в день в течение 14 дней. Каждая таблетка содержала 200 мг лопинавира (плюс 50 мг ритонавира для замедления печеночного клиренса лопинавира). Других форм препарата не было, поэтому пациенты на ИВЛ не получали лопинавир, будучи не в состоянии глотать.
- интерферон (в основном подкожно): 3 дозы в течение 6 дней по 44 мкг подкожно Интерферон-β1a;
Там, где был доступен внутривенный интерферон, пациенты, получавшие высокопоточную назальную оксигенотерапию, находящиеся на ИВЛ или ЭКМО (Extracorporeal membrane oxygenation - экстракорпоральная мембранная оксигенация), вместо этого должны были получать 10 мкг внутривенно 1 раз в день в течение 6 дней.
Конечные точки
Основная цель, указанная в протоколе, заключалась в оценке влияния на госпитальную смертность (т.е. смертность во время первоначального эпизода госпитализации; последующее наблюдение прекращалось при выписке) не только у всех пациентов, но и у пациентов с умеренным и тяжелым течением COVID-19 (впоследствии определяемые как находящиеся на ИВЛ при рандомизации).
Вторичными исходами, определяемыми протоколом, были начало проведения ИВЛ и продолжительность госпитализации. Хотя плацебо не использовалось, соответствующий анализ этих несмертельных исходов все же может быть достоверно информативным. Дополнительное исследование CATCO (Canadian Arm of the SOLIDARITY Trial) в Канаде и дополнительное исследование Discovery в Европе (в основном во Франции) зафиксировали дополнительные результаты, о которых будет сообщено в других отчетах.
Размеры выборки
В протоколе говорилось: «Чем больше количество пациентов, тем точнее будут результаты, но это будет зависеть от того, как развивается эпидемия ... возможно ввести в исследование несколько тысяч госпитализированных пациентов с относительно легким течением заболевания и несколько тысяч - с тяжелым течением заболевания. Но реально подходящие размеры выборки не могли быть оценены в начале испытания». Исполнительная группа, не обращая внимания на какие-либо выводы, приняла решение о сроках публикации промежуточных результатов.
Статистический анализ
Анализировалось 4 группы, в которых сравнивались попарно равномерно рандомизированные исследуемый препарат с его контрольной группой. В контрольной группе для тех, кто произвольно получал одно конкретное лекарство, были те пациенты, которым случайным образом могло быть назначено это лекарство (в тот момент, в той больнице), но вместо этого им была назначена стандартная терапия. Если для конкретного участника исследования было доступно более одного исследуемого препарата, то при распределении по стандартной терапии этот пациент попадал бы в контрольную группу для каждого из них. Следовательно, существует частичное перекрытие между 4 контрольными группами. Однако каждое сравнение исследуемого препарата и его контрольных групп является равномерно рандомизированным (50/50) и беспристрастным, поскольку на обе группы в равной степени влияют любые различия между странами или больницами, а также любые временные тенденции в характеристиках пациентов или стандартах оказания медицинской помощи.
Во всех анализах соотносится смертность с назначенным лечением (т.е. они представляют собой анализы назначенного лечения). Общий анализ смертности проводился для всех рандомизированных пациентов (лекарственный препарат против его контрольной группы), и единственный протокол-специфический анализ подгруппы - это те, которые рассматривают отдельно пациентов с умеренным и тяжелым течением COVID-19 (т.е. уже находящихся на ИВЛ; тип вентиляции не был зарегистрирован при входе в исследование.) Нестратифицированные методы Каплана-Мейера определяют 28-дневный риск выживаемости. Коэффициенты смертности (RR) и значения p взяты из логарифмического анализа, стратифицированного для 3x2 = 6 слоев возраста и проведения ИВЛ на момент поступления. Если стратифицированный логарифмический анализ Наблюдаемое минус Ожидаемое количество смертей составляет O-E с дисперсией V, logeRR рассчитывается как (O-E)/V с дисперсией 1/V и нормальным распределением. [8] Несколько неопределенных в настоящее время значений времени смерти были приняты за 7-й день. Исследованы цензурированные пациенты с результатами, которые еще не были сообщены в день 0, и цензурированы несколько переводов между больницами. Они не подвергали цензуре пациентов, выписанных живыми, поскольку анализировался уровень смертности во время первой госпитализации. Форест-плот (с 95% доверительным интервалом только для общих результатов, в противном случае - с 99% доверительным интервалом) и статистика хи-квадрат (сумма [O-E]2/V, без значения p) помогают интерпретировать любую очевидную гетерогенность RR лечения между подгруппами. В анализах использовались программы SASv9.4 и Rv4.02.
Обсуждение включает метаанализ результатов основных испытаний, основанный на средневзвешенном значении обратной дисперсии b = logeRR для каждой страты каждого исследования, с использованием отношения шансов, когда данные о соотношении рисков или смертности отсутствуют. (Это средневзвешенное значение получается из сумм [O-E] и V по стратам. [8]) В целом, чем больше смертей в страте, тем больше V и, соответственно, меньше дисперсия logeRR, поэтому тем больше вес этот слой получает. Дисперсия, приписываемая результату в каждой страте и общему средневзвешенному значению, отражает только случайность при рандомизации. Однородность различных RR не требуется, чтобы это средневзвешенное значение было информативным.
Надзор и финансирование
Исследование зарегистрировано (ISRCTN83971151, NCT04315948), протокол одобрен локальным комитетом по этике и комитетом ВОЗ по этике. Проведение исследования соответствует Хельсинкской декларации и принципам надлежащей клинической практики, а также национальным правилам проведения исследований. Формы согласия подписывались и сохранялись пациентами и отмечались в документации. Согласие, как правило, было проспективным, но могло (при наличии локального одобрения) быть ретроспективным. Единственным исключением были пациенты без четкого согласия на последующее наблюдение. Были включены все остальные рандомизированные пациенты («анализ намерения лечить»). ВОЗ является глобальным ко-спонсором, а правительства - ко-спонсорами на национальном уровне, а управление испытаниями осуществляет Исполнительная группа (EG - International Steering Committee’s Executive Group) Международного руководящего комитета. Внешний статистический анализ для независимого комитета по мониторингу данных и безопасности (Data and Safety Monitoring Committee - DSMC) не проводился ни EG, ни ВОЗ, за двумя исключениями. После внешних доказательств бесполезности гидроксихлорохина и лопинавира, EG запросила их неслепой анализ. Затем, с последующим решением ослепить сообщение обо всех промежуточных результатах, EG отредактировала эту рукопись, составленную группой исследований ВОЗ и внешними статистиками.
Страны-участницы покрыли почти все локальные расходы, а ВОЗ покрыла все остальные расходы на исследования, не получая дополнительного финансирования. Сотрудники, члены комитетов, аналитики данных и системы управления данными не взимали никаких затрат, а лекарства были переданы в дар. Ни один донор не оказал необоснованного (см. конечный материал) влияния на анализ, подготовку рукописи или ее подачу. Записывающая группа ручается за правильность протокола, точность и полноту данных.
Результаты
С 22 марта по 4 октября 2020 г. было госпитализировано 11330 пациентов в 405 больницах 30 стран во всех 6 регионах ВОЗ. Из них 64 (0,6%) не имели согласия (или не были уверены в своем решении его дать) на последующее наблюдение. В исследовании осталось 11 266 пациентов: 2750 получили ремдесивир, 954 гидроксихлорохин, 1411 только лопинавир-ритонавир, 2063 интерферон и 4088 стандартную терапию. (рисунок 1; отчетность составляет 97% для тех, кто вошел в исследование> 1 месяц назад, и 99,7% для тех, кто вошел> 3 месяца назад). Все 3 пациента с отрицательным результатом на COVID-19 были включены в исследование и выжили. В таблице 1 представлены характеристики пациентов: 9120 (81%) возраст <70 лет, 6985 (62%) мужчины, 2768 (25%) больные диабетом, 916 (8%) находящихся на ИВЛ и 7002 (62%) рандомизированных в дни 0-1. Для каждого препарата характеристики пациентов были хорошо сбалансированы нестратифицированной рандомизацией 50/50 между ним и его контролем. Смерть наступала в среднем на 8-й день (IQR 4-14), выписка - на 8-й день (IQR 5-13). При 1253 смертельных исходах оценка 28-дневной смертности по оценке Каплана Мейера составила 11,8%. Этот риск зависел от нескольких факторов, в частности от возраста (20%, если ≥70 лет, 6%, если <50 лет) и ИВЛ (39% при ИВЛ, в противном случае 10%). Таблица 1 также описывает соответствие. Для ремдесивира запланированный период лечения составлял 10 дней (или до предшествующей смерти или выписки). Из тех, кому был назначен Ремдесивир, 98,5% начали лечение. В середине этого периода 96% все еще принимали его (по сравнению только с 2% в группе контроля ремдесивира). Аналогичным образом, для других препаратов комплаентность была высокой (94–95%), а перекрестная - низкой (2–6%). Изучение лечения прекратилось по графику. Абсолютные различия между лечением и контролем при использовании кортикостероидов и другой стандартной терапии были небольшими (таблица S2). Для каждого попарного сравнения лекарств на рис. 2 представлен нестратифицированный анализ Каплана-Мейера 28-дневной внутрибольничной смертности (перечисленные ниже числа на оси X подвергаются риску и умирают каждую неделю, а числа умирающих - после 28-го дня), а также коэффициенты смертности RR стратифицированы по возрасту и проведению ИВЛ. На рис. 3 показаны RR в подгруппах по возрасту, стратифицированных по проведению ИВЛ и по возрасту + ИВЛ, а также общие RR, стратифицированные по обоим параметрам.
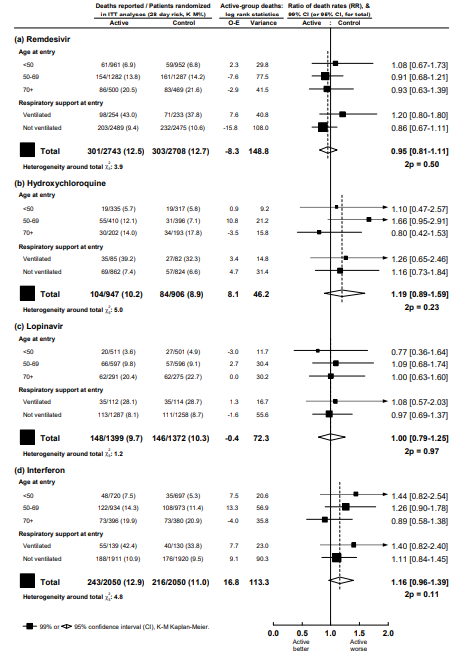
Взяв вместе рисунки 2 и 3, ни один исследуемый препарат не оказал определенного влияния на смертность ни в целом (каждый p>0,10), ни в какой-либо подгруппе, определяемой возрастом или ИВЛ на момент поступления (или другими характеристиками при поступлении, или географическим регионом, или применением кортикостероидов: рисунки S6-S9). Коэффициенты смертности (ДИ (confidence interval - доверительный интервал) 95% и зарегистрированным на данный момент числом смертей при приеме препаратов или в контрольной группе) составили:
- RR ремдесивира = 0,95 (0,81-1,11, p = 0,50; 301/2743 против 303/2708),
- RR гидроксихлорохина = 1,19 (0,89 -1,59, p = 0,23; 104/947 против 84/906),
- RR лопинавира = 1,00 (0,79-1,25, p = 0,97; 148/1399 против 146/1372) и
- RR интерферона = 1,16 (0,96-1,39, p = 0,11 ; 243/2050 против 216/2050).
Нестратифицированные сравнения дали аналогичные нулевые результаты (рис. 2), как и анализы, исключающие пациентов, принимающих кортикостероиды, и многомерный анализ чувствительности, оценивающий одновременно эффекты всех 4 исследуемых препаратов (таблица S3). Если ИВЛ препятствует пероральному введению лопинавира или других исследуемых препаратов, это может снизить любое влияние на смертность от назначения этих препаратов, но заранее запланированные анализы смертности у пациентов, еще не находящихся на ИВЛ при поступлении, также показали отсутствие определенного защитного эффекта от любого исследуемого препарата (рисунок 3). Предварительно запланированными результатами исследования были смерть, проведение ИВЛ и время выписки. Ни один из исследуемых препаратов не уменьшал количество инициирования ИВЛ у тех, кто еще не находился на ИВЛ. Цифры, исследуемого препарата по сравнению с контролем, с проведением ИВЛ, инициированной после рандомизации, были следующими: ремдесивир 295v284, гидроксихлорохин 75v66, лопинавир 124v119, интерферон 209v210 (таблица S1). В этом открытом исследовании пациенты, которых можно было бы считать готовыми к выписке, могли задерживаться несколько дольше только потому, что им давали исследуемый препарат, но эту трудность можно обойти. Каждое из 3 исследуемых курсов лечения, рассчитанное на срок > 7 дней, увеличивало процентное содержание, остающихся в больнице на 7-й день. Если у одного из этих 3 препаратов наблюдалось ускоренное выздоровление, то размеры этого увеличения должны были отличаться, но они не изменились: увеличение было поразительно аналогичным. Процент пациентов, все еще госпитализированных на 7-й день (исследуемый препарат по сравнению с контролем): ремдесивир 69% против 59%, гидроксихлорохин 64% против 54%, лопинавир 68% против 59% (таблица 1). Информативный с медицинской точки зрения результат - отсутствие какой-либо существенной разницы между этими тремя прибавками. Дополнительные анализы по распределению лечения (таблицы S2-S3, рисунки S2-S9) сводят в таблицу сопутствующие лекарства (обнаруживают только небольшие абсолютные различия), обеспечивают многомерную регрессию Кокса, подходящую для всех 4 препаратов одновременно (с получением RR смертности, как на рисунке 3), подразделяют 28-дневные графики смертности (как на рисунке 2) по ИВЛ при поступлении и дают анализ RR смертности по подгруппам по многим характеристикам пациентов и по применению кортикостероидов (не выявляя примечательных подгрупповых или географических изменений). Все активное лечение закончилось в течение ≤14 дней, и количество смертей в течение этого 14-дневного периода с связанное любой сердечной причиной, указанной в электронной записи о смерти, составляло ремдесивир 7v8, гидроксихлорохин 4v2, лопинавир 6v3 и интерферон 6v8 (рисунок S11). Хотя многие смерти от COVID-19 были связаны с полиорганной недостаточностью, смерть от приема исследуемого препарата не была связана с поражением почек или печени.
Обсуждение
Основные исходы, такие как летальность, начало проведения ИВЛ и продолжительность госпитализации, не были четко сокращены ни одним из исследуемых препаратов. Данные о смертности не могли быть существенно искажены из-за открытого дизайна без плацебо или из-за вариаций характеристик пациентов или стандартной терапии. Маловероятно, что влияние на начало проведения ИВЛ было существенно предвзято, и хотя прием препаратов в течение 10 дней может задержать выписку пациента, поразительное сходство этой задержки с 3 различными ежедневными приемами лекарства свидетельствует о том, что ни одно из них не имело фармакологического эффекта, который заметно сокращает время до выздоровления. Хотя в исследовании Adaptive COVID-19 Treatment Trial (ACTT-1) в сочетании с плацебо-контролем сообщалось, что ремдесивир умеренно сокращает время до выздоровления, в настоящем исследовании не было существенного влияния на начало применения ИВЛ или время до выписки.
Основная цель заключалась в том, чтобы помочь определить, может ли какой-либо из 4 перепрофилированных противовирусных препаратов хотя бы умеренно повлиять на внутрибольничную смертность и есть ли различия в эффектах при умеренном и тяжелом течении заболевания. Результаты следует рассматривать в контексте всех данных о смертности, полученных в результате должным образом рандомизированных исследований, но для ремдесивира и Интерферона это исследование дает более 3/4 этих доказательств.
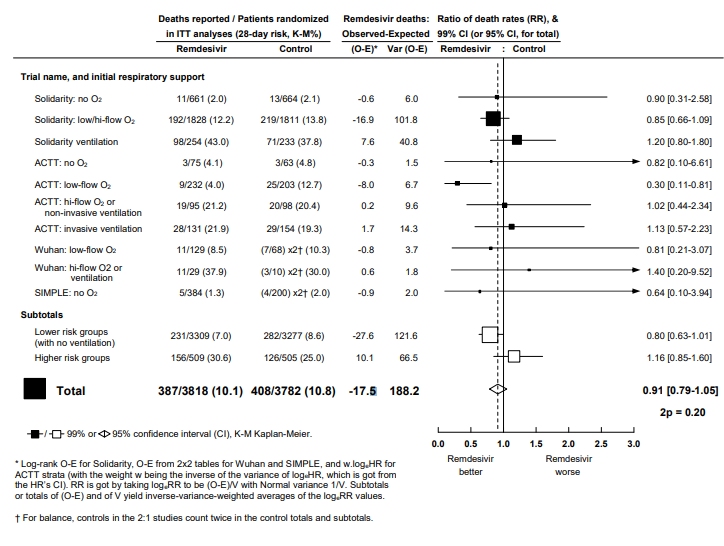
Было проведено 4 испытания включающих ремдесивир по сравнению с тем же лечением без него: Solidarity (604 смерти из примерно 5000 рандомизированных), ACTT-1 (136 смертей примерно из 1000) и два меньших испытания (41 смерть) [5,6,7]. На рисунке 4 представлены результаты смертности при анализе каждого испытания, с разбивкой по начальной респираторной поддержке. (Эти сравнения “подобного с подобным” позволяют предположить, что пропорция, уже получающая высокопоточную назальную оксигенотерапию или ИВЛ на момент начала исследования ACTT-1, была, случайно, несколько ниже для ремдесивира, чем для плацебо.) При соответствующем объединении данных из всех 4 испытаний, [8] Коэффициент смертности ремдесивира по сравнению с контрольной группой составляет 0,91 (95% ДИ 0,79–1,05).
Интерпретация должна в основном отражать не значение p (p = 0,21) или точечную оценку (RR = 0,91), а доверительный интервал (0,79-1,05), который показывает диапазон коэффициентов смертности, комфортно совместимый со средневзвешенным значением результатов всех испытаний. Это абсолютно исключает предположение, что ремдесивир может предотвратить значительную часть всех смертей. Доверительный интервал удобно совместим с предотвращением небольшой части всех смертей, но также удобно совместим с предотвращением отсутствия смертей (что согласуется с очевидным отсутствием эффекта ремдесивира на начало проведения ИВЛ или продолжительности госпитализации в исследовании Solidarity).
Статистические неопределенности намного больше, если внимание ограничивается конкретными подгруппами или периодами времени [9]. Если ремдесивир не влияет на смертность, то случай может дать несколько благоприятные результаты в подгруппе результатов всех испытаний, с более поразительными результатами в выбранной подгруппе конкретного испытания (как в одной подгруппе ACTT-1, где коэффициент смертности оказался 0,30: рисунок 4). Хотя как ACTT-1, так и Solidarity предполагали возможность получения различных степеней пользы у пациентов с низким и высоким риском, конкретное подразделение результатов ACTT-1 на рис. 4 было незапланированным. (Протокол ACTT-1 определил отдельные анализы тех, кто не нуждался в кислороде: только 3/75 против 3/63 смертей в ACTT1, 11/661 против 13/664 в Solidarity и 5/384 против 4/200 в SIMPLE; общий RR = 0,82, но с широким доверительным интервалом 0,43-1,55.). Таким образом, хотя промежуточные итоги всех испытаний на рисунке 4 предполагают некоторую пользу у пациентов с низким риском и некоторую опасность у стационарных пациентов с высоким риском (с абсолютной пользой для пациентов с низким риском) кажущийся несколько меньшим, чем абсолютный риск в группе высокого риска), ни один промежуточный итог не следует рассматривать отдельно от другого промежуточного итога или от ДИ для общего.
В отношении гидроксихлорохина и лопинавира в исследовании «Solidarity» не обнаружилось определенных доказательств пользы или риска в какой-либо подгруппе. Единственное другое существенное испытание этих двух препаратов - это «Recovery» [10,11], которое для этих препаратов больше, чем «Solidarity». Комбинация лог-рангового анализа этих двух относительно крупных испытаний (с помощью методов метаанализа, использованных на рисунке 4) объединяет результаты обоих. Для гидроксихлорохина относительный риск совместной смертности (при объединении двух испытаний) составил 1,11, 95% ДИ 0,99–1,24, без явной пользы независимо от проведения ИВЛ или без нее. Этот ДИ исключает какую-либо существенную выгоду от этой схемы гидроксихлорохина у пациентов, госпитализированных для лечения COVID-19. Он совместим с некоторой опасностью, но не демонстрирует опасности. Несмотря на опасения, что ударная доза может быть временно кардиотоксичной, ни в одном испытании не наблюдалось повышенной смертности в течение первых нескольких дней, когда уровни в крови были самыми высокими. Ни в одном испытании не регистрировалась доза / кг, ожирение или параметры ССС, а количество смертей от сердечно-сосудистых причин было слишком мало, чтобы быть достоверно информативным. Недавний метаанализ выявил 27 небольших рандомизированных испытаний гидроксихлорохина (всего 167 смертей, RR = 1,00, 0,71–1,42); [12], объединяющих все 29 испытаний, RR = 1,10, 0,99–1,22, опять же без учета какой-либо материальной выгоды. Для лопинавира (всегда вводимого одновременно с ритонавиром) RR совместной смертности (объединяя исследования Solidarity, Recovery и единственное информативное небольшое исследование [13]) составило 1,02, 95% ДИ 0,91–1,14. Хотя таблетки лопинавира нельзя было проглотить пациентам, находящимися на ИВЛ, не было очевидной пользы в анализах, ограниченных теми, которые еще находились на ИВЛ при поступлении. Этот ДИ указывает на отсутствие существенного влияния на смертность и исключает пропорциональное снижение на 10%. Дополнительное исследование, проведенное в рамках Solidarity, Discovery, зафиксировало многие клинические параметры, выявив неожиданное повышение креатинина (возможно, из-за того, что уровни в крови выше, чем у пациентов с аналогичными дозами при ВИЧ [14,15]), но Solidarity и Recovery не зафиксировали ни одной смерти от поражения печени и почек связанных приемом лопинавира.
В отношении интерферона-β1a не сообщалось о крупных исследованиях смертности. На основе данных примерно 4000 пациентов RR смертности в исследовании Solidarity составил 1,16, 0,96 1,39; p = 0,11 (или 1,12, 0,83–1,51, без одновременного применения лопинавира: рисунок S9). Это не демонстрирует опасности, но нижний предел достоверности исключает умеренное снижение смертности при этих обстоятельствах. Около половины пациентов, получавших интерферон (и половина их контрольной группы), получали кортикостероиды, [16] но соотношение RR интерферона и контрольной смертности, казалось, не зависело от приема кортикостероидов. Большая часть интерферона вводилась подкожно, а интерферон, вводимый подкожно и внутривенно, имел разную фармакокинетику, [17] но клиническое значение этого неясно. Рандомизация к интерферону прекращается в исследовании Solidarity 16 октября, но появятся и другие доказательства: сообщение о том, что ингаляционный интерферон-β1a может быть высокоэффективным, охватывал только около 100 пациентов с COVID-19 (NCT04385095), но продолжающееся плацебо-контролируемое исследование подкожного введения ACTT-3 Интерферон-β1a стремится задействовать 1000 (NCT04492475). Для каждого из этих 4 перепрофилированных неспецифических противовирусных препаратов несколько тысяч пациентов были рандомизированы в различные исследования. Бесперспективных общих результатов проверенных схем достаточно, чтобы опровергнуть ранние надежды, основанные на небольших или нерандомизированных исследованиях, что любое из них существенно снизить госпитальную смертность, начало проведения ИВЛ или продолжительность госпитализации. Было бы полезно использовать более узкие доверительные интервалы (особенно для ремдесивира), но основная потребность заключается в улучшении лечения. Solidarity все еще набирает около 2000 пациентов в месяц, и эффективные факторные дизайны позволят оценить дальнейшие методы лечения, такие как иммуномодуляторы и специфические моноклональные антитела против SARS-CoV-2.
Благодарности
Главный исследователь выражает признательность тысячам пациентов и их семей, которые участвовали в этом испытании, а также сотням медицинских работников, которые рандомизировали пациентов и заботились о них. Министерства здравоохранения участвующих государств-членов и их национальные учреждения оказали важную поддержку в реализации исследования. Отдельное внимание стоит уделить Группе авторов, не обязательно ВОЗ. NJ White et al [4] предоставили неопубликованные данные о фармакокинетике гидроксихлорохина, результаты исследования Recovery [10,11] с общей статистикой логарифмических рангов, результаты исследования ACTT-1 [5] по соотношению рисков общих подгрупп, а Bin Cao поделился подробностями исследования в г. Ухане [6]. Подготовка, проверка и отправка MS контролировались исследовательской группой ВОЗ и комитетом по написанию. Для основного исследования Solidarity спонсоров не было, но дополнительное исследование Discovery получило грант программы исследований и инноваций EU Horizon 2020 101015736. Страны-участницы покрыли почти все локальные расходы, а ВОЗ покрыла все другие расходы на исследования, не получая дополнительного финансирования. Сотрудники, члены комитетов, аналитики данных и системы управления данными не взимали никаких затрат, а лекарства были переданы в дар. Castor EDC пожертвовал и управлял своей облачной системой сбора клинических данных и управления ими, не обращая внимания на результаты исследований. Обработка и анализ анонимных данных проводились университетами Берна, Бристоля и Оксфорда. Ремдесивир был предоставлен фармкомпанией Gilead Sciences, гидроксихлорохин - Mylan, лопинавир - Abbvie, Cipla и Mylan, а интерферон β1a - Merck KGaA (подкожно) и Faron (внутривенно).
Литература
- World Health Organization, R&D Blueprint. A coordinated global research roadmap: 2019 novel coronavirus. (Скоординированная глобальная дорожная карта исследований: новый коронавирус 2019 года) Geneva, Switzerland March 2020 who.int (accessed October 3, 2020).
- World Health Organization, R&D Blueprint. Informal consultation on prioritization of candidate therapeutic agents for use in novel coronavirus 2019 infection (Неофициальная консультация по определению приоритетов потенциальных терапевтических агентов для использования при новой коронавирусной инфекции 2019 года) who.int (accessed October 3, 2020).
- World Health Organization, R&D Blueprint. An international randomised trial of additional treatments for COVID-19 in hospitalised patients who are all receiving the local standard of care (Международное рандомизированное исследование дополнительных методов лечения COVID-19 у госпитализированных пациентов, которые все получают местный стандарт медицинской помощи) who.int (accessed October 3, 2020).
- White NJ, Watson JA, Hoglund RM, Chan XHS, Cheah PY, Tarning J. COVID-19 prevention and treatment: A critical analysis of chloroquine and hydroxychloroquine clinical pharmacology. (Профилактика и лечение COVID-19: критический анализ клинической фармакологии хлорохина и гидроксихлорохина) PLoS Med 2020;17(9):e1003252. doi.org
- Beigel JH, Tomashek KM, Dodd LE, et al. Remdesivir for the treatment of Covid-19 — preliminary report. (Ремдесивир для лечения COVID-19 — предварительный отчет.) N Engl J Med 2020 doi:10.1056/NEJMc2022236 doi.org
- Wang Y, Zhang D, Du G, et al. Remdesivir in adults with severe COVID-19: a randomised, doubleblind, placebo-controlled, multicentre trial. (Ремдесивир у взрослых с тяжелой формой COVID-19: рандомизированное, двойное слепое, плацебо-контролируемое многоцентровое исследование) Lancet 2020;395:1569-78. doi.org
- Spinner CD, Gottlieb RL, Criner GJ, et al. Effect of Remdesivir vs Standard Care on Clinical Status at 11 Days in Patients With Moderate COVID-19: A Randomized Clinical Trial. (Рандомизированное Клиническое Исследование) JAMA. 2020;324(11):1048-57. doi:10.1001/jama.2020.16349 doi.org
- Early Breast Cancer Trialists’ Collaborative Group (EBCTCG). Effects of chemotherapy and hormonal therapy for early breast cancer on recurrence and 15-year survival: an overview of the randomised trials. (Влияние химиотерапии и гормональной терапии раннего рака молочной железы на рецидив и 15-летнюю выживаемость: обзоррандомизированныхисследований) Lancet 2005; 365: 1687–1717. All rights reserved. No reuse allowed without permission. (which was not certified by peer review) is the author/funder, who has granted medRxiv a license to display the preprint in perpetuity. medRxiv preprint doi: doi.org; this version posted October 15, 2020. The copyright holder for this preprint 12
- Peto R. Current misconceptions: that subgroup-specific trial mortality results often provide a good basis for individualising patient care. (Современные заблуждения: результаты исследований смертности в конкретных подгруппах часто служат хорошей основой для индивидуализации ухода за пациентами) British Journal of Cancer (2011) 104, 1057-58 doi:10.1038/bjc.2011.79 doi.org
- RECOVERY collaborative group. Effect of hydroxychloroquine in hospitalized patients with COVID19. (Влияние гидроксихлорохина на госпитализированных пациентов с COVID-19) N Engl J Med DOI: 10.1056/NEJMoa2022926 doi.org (online October 8, 2020)
- RECOVERY Collaborative Group. Lopinavir–ritonavir in patients admitted to hospital with COVID-19 (RECOVERY): a randomised, controlled, open-label, platform trial. (Лопинавир–ритонавир у пациентов, поступивших в больницу с COVID-19 (восстановление): рандомизированное, контролируемое, открытое,платформенное исследование) Lancet DOI: doi.org (Online October 5, 2020)
- Axfors C, Schmitt AM, Janiaud P, et al. Mortality outcomes with hydroxychloroquine and chloroquine in COVID-19: an international collaborative meta-analysis of randomized trials. (Летальные исходы при применении гидроксихлорохина и хлорохина в COVID-19: международный совместный метаанализ рандомизированных исследований) medRxiv preprint, posted September 18, 2020. doi: doi.org
- Cao B, Wang Y, Wen D, et al. A trial of Lopinavir-Ritonavir in adults hospitalized with severe Covid19. (Исследование Лопинавира-ритонавира у взрослых, госпитализированных с тяжелой формой COVID-19) N Engl J Med 2020;382:1787-99. doi:10.1056/NEJMoa2001282 doi.org
- Venisse N, Peytavin G, Bouchet S et al. Concerns about pharmacokinetic (PK) and pharmacokineticpharmacodynamic (PK-PD) studies in the new therapeutic area of COVID-19 infection. (Озабоченность по поводу фармакокинетических и фармакокинетико-фармакодинамических исследований в новой терапевтической области инфекции COVID-19). doi.org Antiviral Res 181 (2020) 104866
- Gregoire N, Le Turnier P, Gaborit BJ ey al. Lopinavir pharmacokinetics in COVID-19 patients. (Фармакокинетика лопинавира у пациентов с COVID-19). J Antimicrob Chemother doi:10.1093/jac/dkaa195. doi.org
- Jalkanen J, Pettilä V, Huttunen T, et al. Glucocorticoids inhibit type I IFN beta signaling and the upregulation of CD73 in human lung. (Глюкокортикоиды ингибируют сигнализацию IFN бета I типа и повышают регуляцию CD73 в легких человека). Inten Care Med 2020 Oct;46(10):1937-40. doi: 10.1007/s00134- 020-06086-3 doi.org
- Jalkanen J, Hollmén M, Jalkanen S. Interferon beta-1a for COVID-19: critical importance of the administration route. (Интерферон бета-1а для COVID-19: критическая важность пути введения). Crit Care 2020;24:Article 335. doi: 10.1186/s13054-020-03048-5 doi.org
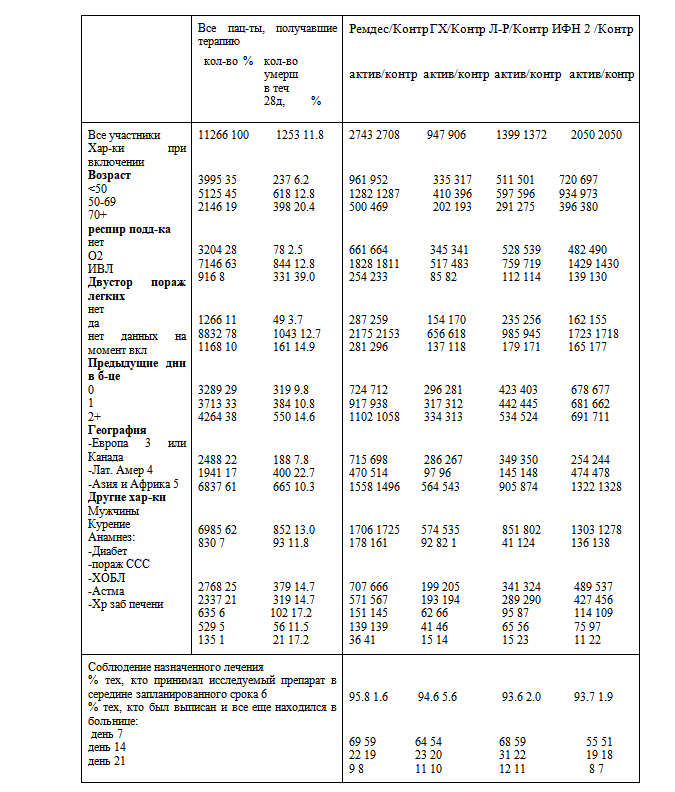
Таблица 1. Характеристики входа путем случайного распределения и соответствие этому распределению.
Исключая 64 пациентов без четкого согласия на последующее наблюдение. Сравнение каждого исследуемого препарата с одновременным назначением одного и того же лечения без него. Поскольку контрольные группы пересекаются, общее количество (11 266) меньше суммы чисел в парных сравнениях.
Примечания: Некоторые неизвестные с определенной характеристикой объединяются с самой большой категорией этой характеристики.
- «28-дневный KM%» - это 28-дневный % риска смерти во время госпитализации по Каплану-Мейеру. Категория «Умерли» включает в себя любые случаи смерти в больнице после 28-го дня.
- Рандомизация интерферона: интерферон + лопинавир против лопинавира до 4 июля, затем интерферон против стандартной терапии.
- Албания, Австрия, Бельгия, Финляндия, Франция, Ирландия, Италия, Литва, Люксембург, Македония, Норвегия, Испания, Швейцария.
- Аргентина, Бразилия, Колумбия, Гондурас, Перу.
- Египет, Индия, Индонезия, Иран, Кувейт, Ливан, Малайзия, Пакистан, Филиппины, Саудовская Аравия, Южная Африка.
- Комплаентность рассчитывается только среди тех, кто умер или был выписан живыми, и определяется как процент приема исследуемого препарата в середине его запланированной продолжительности (или в середине времени от поступления до смерти или выписки, если это меньше).
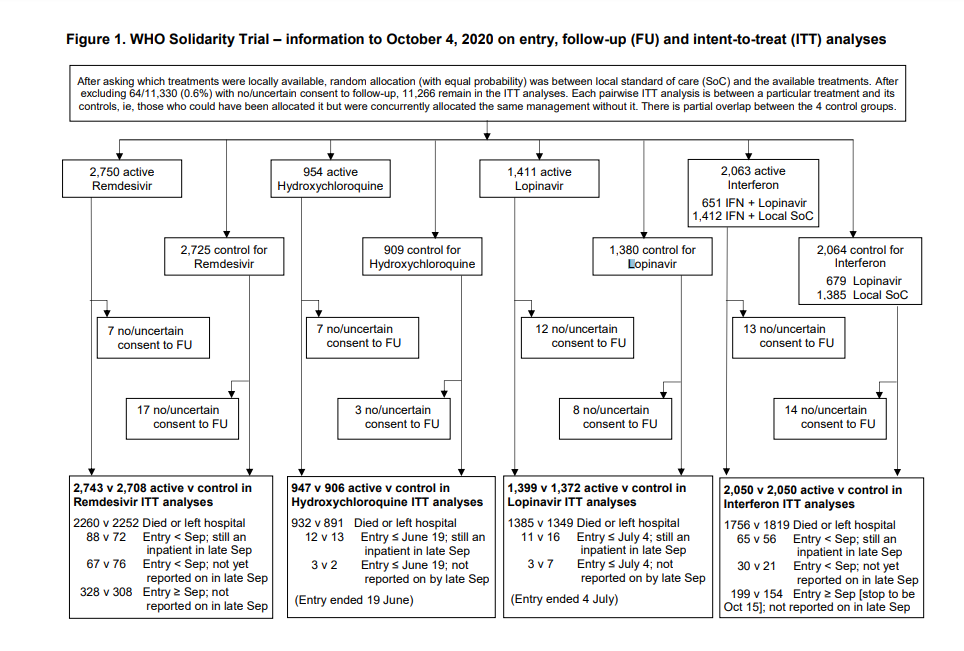
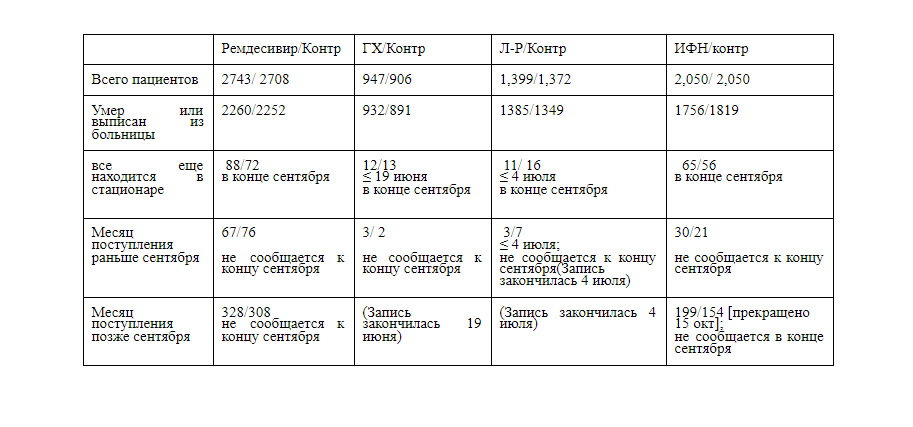
Рисунок 1. После выяснения того, какие виды лечения были доступны на локальном уровне, было произведено случайное распределение (с равной вероятностью) между местной стандартной терапией (SoC) и доступными видами лечения. После исключения 64/11330 (0,6%) с отсутствующим / неопределенным согласием на последующее наблюдение, 11 266 остаются в анализе ITT. Каждый попарный ITT-анализ проводится между конкретным лечением и его контрольной группой, т. е. Теми, кому оно могло быть назначено, но одновременно им было назначено такое же лечение без него. Есть частичное совпадение между 4 контрольными группами.
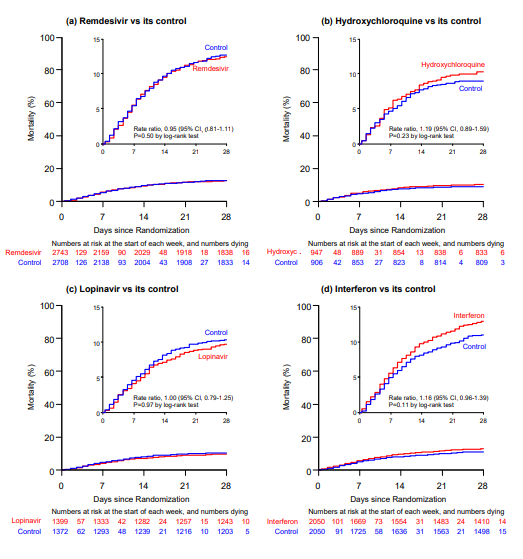
Рисунок 2. Эффекты (а) ремдесивира, (б) гидроксихлорохина, (c) лопинавир и (d) интерферон на 28-дневную смертность.
Графики Каплана-Мейера по внутрибольничной смертности. На вставке те же данные показаны на развернутой оси ординат (нет различий в группе препаратов и контрольной группе).
Рисунок 3. Коэффициенты смертности, стратифицированные по возрасту и респираторной поддержке при поступлении, (a) Ремдесивир, (b) Гидроксихлорохин, (c) Лопинавир, (d) Интерферон, каждый по сравнению с его контрольным препаратом.
Рисунок 4. Ремдесивир против контроля - метаанализ смертности в исследованиях случайного распределения госпитализированных пациентов с COVID-19 на Ремдесивир или такое же лечение без него.
Log-rank O-E для Solidarity, O-E из таблиц 2x2 для г.Ухань и SIMPLE и w.logeHR для страт ACTT (с весом w, обратным дисперсии logeHR, полученной из ДИI HR). RR получается, принимая logeHR равным (O-E)/V с нормальной дисперсией 1/V. Промежуточные итоги или итоги (O-E) и V дают взвешенные с обратной дисперсией средние значения logeHR.
Для баланса контроль в исследованиях 2:1 учитывается дважды в заключительных итогах и промежуточных итогах.