Обзор диагностических тестов для диагностики COVID-19

Оригинал: FDA
Авторы: FDA
Опубликовано: 16 ноября 2020, FDA
Перевод: Константин Сергеев, Фонд “Не напрасно!”
Редакция: Дмитрий Сергеев, Научный центр неврологии
Управление США по контролю за лекарствами и пищевыми продуктами (FDA) круглосуточно работает над увеличением доступности критически важных медицинских продуктов, включая диагностические тесты, для борьбы с пандемией COVID-19.
На сайте FDA доступен обзор, простым языком объясняющий принципы работы тестов для диагностики COVID-19 и определения антител.
ТЕСТЫ ДЛЯ ДИАГНОСТИКИ COVID-19
При определенных чрезвычайных ситуациях FDA может выдавать разрешение на экстренное применение (emergency use authorization, EUA) для обеспечения ускоренного доступа к критически важным медицинским продуктам, включая лекарственные препараты диагностические тесты. Это может помочь в чрезвычайных ситуациях, когда недоступны альтернативные подходящие и одобренные методы. FDA уже одобрило для экстренного применения множество диагностических тестов для выявления вируса SARS-CoV-2, вызывающего COVID-19.
РАЗРЕШЕНИЕ НА ЭКСТРЕННОЕ ПРИМЕНЕНИЕ
Процесс выдачи разрешения на экстренное применение отличается своей гибкостью от стандарта полной процедуры FDA по выдаче разрешения, допуску или лицензированию. В рамках EUA необходимо подтверждение эффективности продукта и доказательство того, что польза от его применения преобладает над риском. Это позволяет FDA выдавать разрешение на экстренное применение медицинских продуктов, которые соответствуют необходимым критериям, в течение нескольких дней или недель, а не месяцев или лет.
FDA уделяет первоочередное внимание рассмотрению запросов на экстренное применение тестов, которые повышают доступность тестирования или существенно увеличивают его производительность. В соответствии с этим приоритет отдается тестам, которые проводятся на месте оказания помощи (point-of-care); тестам с возможностью сбора материала на дому; тестам, которые полностью проводятся в домашних условиях (от редакции: на данный момент FDA зарегистрирован первый такой тест — молекулярный тест для определения РНК вируса “The Lucira COVID-19 All-In-One Test Kit”, при проведении которого образец из носоглотки помещается в специальный контейнер и примерно через 30 минут с помощью электронного аппарата выдается результат); тестам, снижающим использование расходных материалов; и широко распространенные тесты с высокой производительностью.
ХАРАКТЕРИСТИКИ ТЕСТОВ
Ни один тест не является точным на 100%, и их эффективность может варьировать в зависимости от распространенности заболевания в тестируемой популяции. Тесты для диагностики COVID-19 могут быть менее точными в популяции с низкой распространенностью заболевания и у лиц, не имеющих симптомов, у людей с низким уровнем выделения вируса, или у тех, кого тестируют слишком рано или поздно в ходе развития заболевания.
Тесты оценивают по их чувствительности и специфичности. Чувствительность теста — это доля положительных случаев, которые тест верно определяет как положительные, а специфичность теста — это доля отрицательных случаев, которые тест верно определяет как отрицательные.
- У тестов с высокой чувствительностью обычно отмечается низкая частота ложноотрицательных результатов, однако при их использовании есть риск получения ложноположительных результатов в случае низкой специфичности.
- У тестов с высокой специфичностью обычно отмечается низкая частота ложноположительных результатов, однако при их использовании есть риск получения ложноотрицательных результатов в случае низкой чувствительности.
Для уменьшения влияния ложных результатов все тесты на COVID-19, разрешенные к применению на сегодняшний день, предоставляются только по рецепту врача, чтобы они помогли интерпретировать результаты тестов для пациентов.
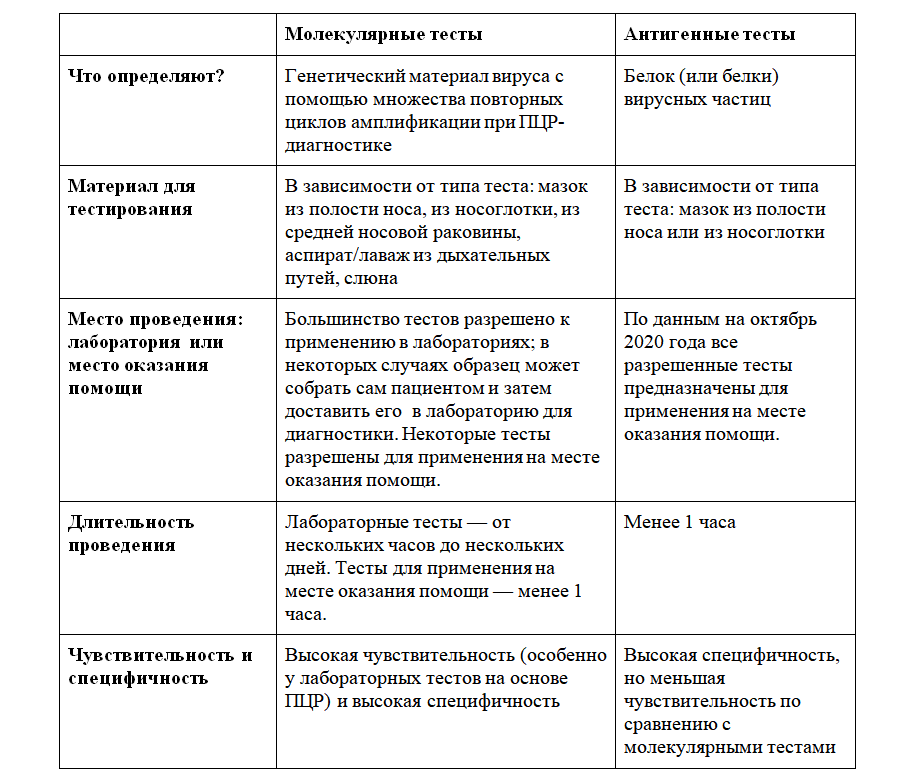
СРАВНЕНИЕ МОЛЕКУЛЯРНЫХ И АНТИГЕННЫХ ТЕСТОВ
Разрешенные к применению в настоящее время диагностические тесты для выявления SARS-CoV-2 работают на основе двух разных принципов. В соответствии с этим выделяют молекулярные и антигенные тесты. Каждый тип теста нацелен на разные части вириона SARS-CoV-2.
- Молекулярные тесты позволяют определить генетический материал или нуклеиновую кислоту, находящиеся внутри вирусной частицы. FDA разрешило применение молекулярных тестов в условиях клинических лабораторий, а также на месте оказания помощи (некоторые тесты). Большинство молекулярных тестов основывается на полимеразной цепной реакции (ПЦР; другое название - тесты, основанные на амплификации нуклеиновых кислот). При ПЦР-диагностике в устройстве, расположенном в лаборатории или на месте оказания помощи, в зависимости от теста, проводится серия реакций. В ходе этих реакций вирусная рибонуклеиновая кислота (РНК), если она присутствует, трансформируется в дезоксирибонуклеиновую кислоту (ДНК), а затем происходит ее амплификация (создаются миллионы копий ДНК), после чего тест выявляет эту ДНК. После нескольких циклов амплификации ПЦР-тесты могут определять даже малое количество вирусного генетического материала в образцах, собранных у пациента, поэтому эти тесты, как правило, обладают высокой чувствительностью (особенно лабораторные ПЦР-тесты). Тест на основе ПЦР может быть разрешен для процесса обработки сгруппированных или объединенных образцов, собранных у пациентов, если разработчик подтвердит соответствие теста стандарту EUA для тестирования объединенных образцов. Если тест объединенных образцов оказался положительным, то каждый образец необходимо протестировать индивидуально для выявления того или тех из них, которые обусловили положительный результат. При низкой распространенности заболевания, когда ожидается большое количество отрицательных результатов, объединение образцов может позволить проводить меньше тестов и использовать меньше расходных материалов.
- Антигенные тесты позволяют определить специфические белки вирусных частиц. Все разрешенные в настоящее время антигенные тесты проводятся на месте оказания помощи и обеспечивают готовность результатов менее чем за час. Антигенные тесты, как правило, обладают высокой специфичностью, но обычно меньшей чувствительностью, чем молекулярные тесты. Однако, поскольку затраты на производство антигенных тестов обычно меньше, чем на молекулярные тесты, и они проще в обращении, то с их помощью масштабы тестирования могут доходить до миллионов людей в день.
Сравнение молекулярных и антигенных тестов для диагностики COVID-19
ЛАБОРАТОРНЫЕ ТЕСТЫ И ТЕСТЫ ДЛЯ ПРОВЕДЕНИЯ НА МЕСТЕ ОКАЗАНИЯ ПОМОЩИ
Большинство диагностических тестов для выявления SARS-CoV-2, разрешенные для экстренного применения, используются в лабораторных условиях, включая некоторые тесты, биоматериал для которых может быть собран самим пациентом с дальнейшей доставкой образца в лабораторию. (От редакции: на момент перевода статьи FDA одобрило первый тест с возможностью сбора материала самим пациентом и диагностики на дому — молекулярный тест для определения РНК вируса “The Lucira COVID-19 All-In-One Test Kit”, при проведении которого образец из носоглотки помещается в специальный контейнер и примерно через 30 минут электронным устройством выдается результат.)
Некоторые диагностические тесты также разрешены для применения на месте оказания помощи, без отправки образцов в лабораторию. Термин “на месте оказания помощи” (point-of-care) подразумевает под собой учреждение для оказания медицинской помощи пациентам, включая:
- Медицинские кабинеты врачей
- Учреждения по длительному медицинскому уходу
- Центры неотложной помощи
- Аптеки
- Кабинет медицинской сестры в школе
- Кабинет врача на производстве
ПОКАЗАНИЯ
Применение диагностических тестов разрешено в соответствии с показаниями, указанными в EUA, которые могут различаться в зависимости от теста. Например, тест может быть разрешен для применения по одной из следующих категорий показаний:
- Разрешены для применения с использованием некоторых типов образцов, собранных у лиц при подозрении или имеющемся COVID-19, при условии появления симптомов COVID-19 в течение заранее обозначенного количества дней до проведения теста.
- Разрешены для применения с использованием некоторых типов образцов, собранных у лиц при подозрении или имеющемся COVID-19 даже при отсутствии симптомов COVID-19.
- Разрешены для применения с использованием некоторых типов образцов, собранных у любого человека, включая лиц без симптомов или других причин, позволяющих заподозрить у них COVID-19. Тесты с таким типом разрешения на применение относятся к тестам для скрининга бессимптомных лиц.
СКРИНИНГ БЕССИМПТОМНЫХ ЛИЦ
Приведенная ниже информация предназначена для работников здравоохранения, которые назначают или проводят тесты для диагностики SARS-CoV-2 у бессимптомных лиц без подозрения на COVID-19.
Имеющиеся данные свидетельствуют о том, что у пациентов с симптомами COVID-19 и бессимптомных лиц без подтвержденного контакта с вирусом количество вирусного генетического материала может не отличаться, однако сведения о распределении вирусной нагрузки среди лиц с симптомами и без них, при различных демографических характеристиках, для различных условий и типов собранных образцов являются ограниченными. Таким образом, при скрининге бессимптомных лиц медицинские работники должны рассмотреть возможность использования тестов с высокой чувствительностью, особенно если доступны тесты с короткими сроками получения результатов. Если высокочувствительные тесты недоступны или если время выполнения диагностики увеличено, то медицинские работники могут рассматривать для использования менее чувствительные тесты, которые можно использоваться на месте оказания помощи, даже если они не имеют специального разрешения для такого показания (т. е. использование “off-label”). Для медицинских организаций по уходу с большим количеством пациентов, таких как учреждения длительного пребывания или аналогичные структуры, многократное проведение быстрых тестов на месте оказания помощи может быть более подходящим вариантом для общего инфекционного контроля по сравнению с менее частым тестированием высокочувствительными методиками с длительным сроком получения результатов.
При использовании тестов для широкомасштабного скрининга бессимптомных лиц, медицинские работники должны быть осведомлены об эффективности тестов и могут рассматривать различные подходы к тестированию, такие как заранее определенный план серийного тестирования или целевое тестирование лиц с высоким риском инфицирования. “Отрицательные” результаты следует рассматривать как “предположительно отрицательные”, а медицинские работники должны оценивать их с учетом данных клинического наблюдения, анамнеза и эпидемиологической информации. Таким образом, при новой значимой вспышке в учреждении по уходу с большим количеством пациентов или при сильном клиническом подозрении на наличие инфекции у конкретного пациента отрицательный результат, полученный при проведении тестирования на месте оказания помощи, в соответствии с рекомендациями CDC, необходимо подтвердить с использованием высокочувствительного молекулярного теста. Нет необходимости проводить подтверждающие молекулярные тесты с высокой чувствительностью у лиц с отрицательным результатом антигенных тестов или других тестов, проводимых на месте оказания помощи, если они получены в рамках рутинного скрининга или эпидемиологического надзора.