Коронавирусная инфекция 2019 (COVID-19): проблемы, связанные с трансплантацией паренхиматозных органов

Оригинал: UpToDate
Авторы: Ajit P Limaye, MD, FACP, FIDSA et al.
Опубликовано: 13 мая 2020, UpToDate
Обновление: 22 января 2021, Наталия Шахгильдян
Перевод: Гузель Рафикова, Фонд профилактики рака
Редакция: Дарья Цыба, Фонд "Не напрасно!"
Краткое содержание
Существует ли риск передачи COVID-19 от донора реципиенту паренхиматозных органов?
Риск передачи SARS-CoV-2 от донора к реципиенту является теоретическим и основан на обнаружении вирусной РНК в органах, которые могут быть пересажены (например, в легких, сердце, почках, кишечнике), и в других биологических субстратах (например, в крови и моче). Тем не менее, на сегодняшний день не зарегистрировано ни одного случая такой передачи SARS-CoV-2.
Необходимо ли проводить скрининг доноров органов и потенциальных реципиентов на COVID-19?
По причине высокого риска передачи SARS-CoV-2, всех доноров органов и потенциальных реципиентов нужно проверять на наличие COVID-19 до забора органов. Основным анализом, используемым для скрининга, является ПЦР мазка (в основном применяется для выявления активной инфекции). Полезность серологии (в основном применяется для выявления перенесенной инфекции) для скрининга перед трансплантацией не установлена.
Имеются ли особенности клинического течения COVID-19 у реципиентов паренхиматозных органов?
Клинические особенности COVID-19 у реципиентов паренхиматозных органов сходны с таковыми у пациентов с ослабленным иммунитетом. Однако лихорадка встречается реже, — возможно, вследствие влияния иммуносупрессивной терапии на системный воспалительный ответ.
Имеются ли особенности диагностики и лечения COVID-19 у реципиентов паренхиматозных органов?
Критерии для тестирования на COVID-19 у реципиентов паренхиматозных органов те же, что и у населения в целом. Однако в их случае у врачей должна быть более высокая настороженность в отношении инфекции, как это обычно рекомендуется для пациентов с ослабленным иммунитетом. Подход к лечению острой инфекции COVID-19 у реципиентов паренхиматозных органов такой же, как и при лечении остальных пациентов, однако следует уделять особое внимание лекарственному взаимодействию и эффектам иммуносупрессивных препаратов.
Следует ли корректировать дозировки иммуносупрессивных препаратов у реципиентов паренхиматозных органов с COVID-19?
Корректировка иммуносупрессивных схем должна быть определена индивидуально, исходя из тяжести заболевания, трансплантированного органа, времени, прошедшего после трансплантации, а также риска острого отторжения аллотрансплантата. Оптимальный подход не определен, авторы рекомендуют снижать дозировки иммуносупрессивной терапии у пациентов, больных COVID-19 в форме от умеренной до тяжелой (например, нуждающихся в госпитализации).
Введение
Реципиенты паренхиматозных органов могут подвергаться повышенному риску заражения COVID-19 из-за иммуносупрессии и частого контакта с системой здравоохранения. Существует также теоретический риск передачи SARS-CoV-2 (вируса, вызывающего COVID-19) при трансплантации органов, хотя на сегодняшний день не описано ни одного случая инфекции, передающейся таким образом.
В этой статье рассматриваются аспекты COVID-19, специфичные для трансплантации паренхиматозных органов, включая скрининг до трансплантации, различные клинические особенности, управление иммуносупрессией и важные взаимодействия лекарств. Другие аспекты лечения COVID-19 обсуждаются отдельно:
- См. Coronavirus disease 2019 (COVID-19): Epidemiology, virology, and prevention (англ.)
- См. Coronavirus disease 2019 (COVID-19): Clinical features and diagnosis (англ.)
- См. Coronavirus disease 2019 (COVID-19): Management in hospitalized adults (англ.)
- См. Coronavirus disease 2019 (COVID-19): Critical care and airway management issues (англ.)
- См. Coronavirus disease 2019 (COVID-19): Issues related to kidney disease and hypertension (англ.)
- См. Coronavirus disease 2019 (COVID-19): Pregnancy issues (англ.)
- См. Coronavirus disease 2019 (COVID-19): Arrhythmias and conduction system disease (англ.)
- См. Coronavirus disease 2019 (COVID-19): Anesthetic concerns, including airway management and infection control (англ.)
Риск передачи
Вероятность донорской инфекции. Риск передачи SARS-CoV-2 от донора к реципиенту является теоретическим и основан на обнаружении вирусной РНК в органах, которые могут быть пересажены (например, в легких, сердце, почках, кишечнике), и в других биологических субстратах (например, в крови и моче) [1-4]. Хотя очевидно, что жизнеспособный вирус может быть культивирован из легких и других частей дыхательного и желудочно-кишечного трактов (ЖКТ), необходимо дополнительное исследование, чтобы определить, является ли SARS-CoV-2 интактным, способным реплицироваться и, следовательно, передается ли при трансплантации других органов.
На сегодняшний день не зарегистрировано ни одного случая донорской инфекции. Точно так же нет и не ожидается информации о передаче вируса через кровь: у SARS-CoV-2 низкая величина и частота виремии [1, 4-6]. (См. Blood donor screening: Medical history, раздел SARS-CoV-2 (no evidence of transfusion-transmitted infection) [англ.])
Посттрансплантационный риск. Неизвестно, выше ли риск заражения SARS-CoV-2 у реципиентов паренхиматозных органов, чем у населения в целом. Тем не менее, хроническая иммуносупрессия может снизить инфекционную дозу, необходимую для того, чтобы вызвать COVID-19, и ослабить иммунный контроль после заражения. Кроме того, реципиенты часто контактируют с системой здравоохранения и, следовательно, потенциально более подвержены воздействию вируса.
Как и другие люди с ослабленным иммунитетом, реципиенты паренхиматозных органов могут выделять большее количество вируса в течение более длительного времени, чем носители, у которых нет дополнительных проблем со здоровьем. Таким образом, они могут с большей вероятностью распространять инфекцию. Необходимы дополнительные данные для подтверждения этих теорий и для количественной оценки вирусной динамики и рисков передачи среди реципиентов паренхиматозных органов.
Откладывание несрочных трансплантаций. Чтобы свести к минимуму риск заражения и сберечь ресурсы больницы, плановая трансплантация (например, трансплантация почки живого донора) и несрочная трансплантация от умершего донора откладываются в некоторых центрах трансплантации, где высока распространенность COVID-19 и/или ограничены ресурсы (не хватает персонала, коек в больнице или отделении интенсивной терапии [ОРИТ], операционных, оборудования) [7-11].
Операции экстренных жизнесохраняющих трансплантаций продолжают выполняться, и медицинские центры США классифицируют трансплантацию органов как деятельность уровня 3b: ее нельзя откладывать, поскольку потенциальные риски нивелируются известными выгодами [12]. Остается неясным, каково соотношение риска и пользы при откладывании плановых трансплантаций в период пандемии. Данные ограничены и свидетельствуют о том, что пациенты, ожидающие пересадку почки, имели более высокий риск госпитализаций и летального исхода по сравнению с теми, кому пересадка была проведена [13]. Постепенно появляются новые данные, свидетельствующие в пользу проведения трансплантации почки во время пандемии, во всяком случае среди определенных групп населения [14].
Скрининг перед трансплантацией
Всех доноров органов и потенциальных реципиентов нужно проверять на наличие COVID-19 до забора органов. Это необходимо, чтобы предотвратить инициирование сильной индукционной иммуносупрессии в контексте активной инфекции, а также чтобы обеспечить безопасность реципиентов (которые, как правило, сильно иммуносупрессированы в период после трансплантации) и команды по забору органов.
Основным анализом, используемым для скрининга, является ПЦР мазка из верхних дыхательных путей (в основном применяется для выявления активной инфекции). Полезность серологии (в основном применяется для выявления перенесенной инфекции) для скрининга перед трансплантацией не установлена. Однако как только показательность серологии для реципиентов паренхиматозных органов будет определена более точно, она может стать полезным вспомогательным анализом. (См. Coronavirus disease 2019 (COVID-19): Clinical features and diagnosis, раздел Microbiologic diagnosis [англ.])
Скрининг доноров. Все доноры должны проходить скрининг на COVID-19 [15]. Обычно мы тщательно собираем анамнез, получаем рентгенограммы или компьютерные томограммы грудной клетки и выполняем микробиологическое тестирование. Во всех случаях решение о трансплантации должно учитывать ургентность операции, а также риски и пользу для каждого пациента. Общие принципы (адаптированы из рекомендаций Американского общества трансплантологии) [16]:
- Трансплантации от доноров с подтвержденным диагнозом или с подозрением на COVID-19 (на основании симптомов или визуализации грудной клетки) в большинстве случаев следует отменять или откладывать.
- Трансплантации от доноров с подтвержденным диагнозом или подозрением на COVID-19 в течение последнего 21 дня в большинстве случаев следует отменять или откладывать.
- Трансплантации от доноров, которые недавно (например, в течение последних 14 дней) контактировали с лицами с подтвержденным или подозреваемым COVID-19, в большинстве случаев следует отменять или откладывать. Однако если у такого донора отрицательный анализ на COVID-19, в отдельных случаях трансплантация может рассматриваться (например, если она экстренно необходима по жизненным показаниям).
- Доноров также следует проверять на наличие инфекции SARS-CoV-2 с помощью ПЦР, проводимой на образцах из дыхательных путей. Подход к скринингу варьирует в зависимости от учреждения и органа, подлежащего пересадке:
- Для умерших доноров органов (особенно доноров легких) рекомендуется проводить скрининг как верхних дыхательных путей (например, брать мазок из носоглотки), так и нижних (например, выполнять бронхоальвеолярный лаваж), поскольку есть данные, свидетельствующие о повышенной чувствительности исследования образцов из нижних дыхательных путей (образцов мокроты, бронхоальвеолярного лаважа) по сравнению с образцами из верхних дыхательных путей.
- Для других доноров скрининг на COVID-19 должен проводиться как минимум на одном образце из верхних дыхательных путей. Необходимость получения серийных образцов и/или образцов нижних дыхательных путей варьирует от центра к центру и часто индивидуальна.
Для живых доноров с положительным результатом на COVID-19 или для умерших доноров, которые перенесли COVID-19, оптимальный период отсрочки неизвестен. Исходя из средней продолжительности выделения вируса (20 дней) [17], Американское общество трансплантологии предлагает подождать не менее 21 дня с момента постановки диагноза и полного разрешения симптомов (для живого донора) до донорства/забора органов [15]. По мере накопления знаний о COVID-19 рекомендации по скринингу будут развиваться.
Проверка кандидатов
Все потенциальные реципиенты органов должны быть до трансплантации проверены на наличие COVID-19 с помощью сбора анамнеза, визуализации органов грудной клетки и микробиологических тестов. Хотя данных недостаточно, COVID-19 может протекать бессимптомно, и есть опасение, что интенсивная иммуносупрессия, проводимая во время трансплантации, может привести к быстро прогрессирующему и потенциально смертельному течению COVID-19.
- Все потенциальные реципиенты должны быть проверены на COVID-19 до трансплантации. В большинстве центров трансплантации это включает ПЦР образца из верхних дыхательных путей (например, мазка из носоглотки), тщательный осмотр и сбор анамнеза, а также визуализацию органов грудной клетки. Для пациентов, у которых отсутствуют респираторные симптомы, обычно достаточно рентгенограммы грудной клетки; для пациентов с респираторными симптомами (даже если они незначительные) подходит компьютерная томография (КТ) грудной клетки.
- Трансплантацию органов кандидатам с активным COVID-19 и/или признаками или симптомами других респираторных заболеваний в большинстве случаев следует откладывать.
Для пациентов с активным COVID-19 и пациентов с положительным результатом скрининга оптимальный период отсрочки неизвестен. Американское общество трансплантологии предлагает подождать, пока все симптомы не исчезнут и как минимум два результата ПЦР на SARS-CoV-2 не будут отрицательными [15]. Как и в случае с любой трансплантацией, если речь идет о пациенте с активным или недавним COVID-19, необходимо взвешивать риски.
Профилактика
Профилактические меры для реципиентов органов аналогичны мерам, определенным для населения в целом (например, социальное дистанцирование, тщательная гигиена рук и дыхательной системы). (См. Coronavirus disease 2019 (COVID-19): Epidemiology, virology, and prevention, раздел Prevention [англ.])
Еще одно соображение заключается в том, что реципиенты паренхиматозных трансплантатов, у которых есть COVID-19, могут выделять большее количество вируса в течение более длительных периодов времени, чем пациенты без иммуносупрессии. Таким образом, может потребоваться более длительная изоляция и/или тестирование для документирования вирусного клиренса, чтобы снизить вероятность распространения инфекции. (См. Coronavirus disease 2019 (COVID-19): Infection control in health care and home settings, раздел Infection control in the home setting и Coronavirus disease 2019 (COVID-19): Infection control in health care and home settings, раздел Discontinuation of precautions [англ.])
Активный COVID-19 в паренхиматозных органах реципиентов
Клиническая картина
Клинические особенности. Клинические особенности COVID-19 у реципиентов паренхиматозных органов различны и сходны с таковыми у пациентов с ослабленным иммунитетом. Однако лихорадка встречается реже, — возможно, вследствие влияния иммуносупрессивной терапии на системный воспалительный ответ [20-24]. Например, в двух сериях случаев, когда у реципиентов паренхиматозных органов в Нью-Йорке наблюдался COVID-19, лихорадка была симптомом только у 58–70% [21,22]. Лимфопения также распространена и может быть более выражена, чем у других пациентов с COVID-19 [22,24]. (См. Coronavirus disease 2019 (COVID-19): Clinical features and diagnosis, раздел Clinical features [англ.])
Тяжесть заболевания. Неясно, имеют ли реципиенты трансплантатов более высокий риск развития тяжелой формы COVID-19 по сравнению с инфицированными пациентами, не подвергшимися трансплантации органов. У многих реципиентов есть сопутствующие заболевания (например, гипертоническая болезнь, сахарный диабет, хроническая болезнь почек, сердечно-сосудистые заболевания), которые связаны с более тяжелым течением COVID-19 и более высокой смертностью, что затрудняет оценку того, как трансплантация органов влияет на тяжесть заболевания.
В то время как результаты некоторых исследований свидетельствуют о более высоком уровне смертности среди пациентов, которым была произведена трансплантация солидных органов [21, 22, 24-31], данные между исследованиями различаются [32-35]. В одном многоцентровом когортном исследовании проводилось сравнение двух групп пациентов: 98 реципиентов паренхиматозных органов, поступивших в отделения реанимации и интенсивной терапии (ОРИТ), и пациентов, подобранных в контрольную группу. Исследование показало, что частота искусственной вентиляции легких (ИВЛ), острого респираторного дистресс-синдрома (ОРДС), назначения вазопрессорных препаратов и развития летальных исходов были сопоставимы в обеих группах [34]. В другом исследовании проводилось сравнение 45 реципиентов паренхиматозных органов с 2427 пациентами той же сети больниц, которым трансплантация не проводилась. Было показано, что у реципиентов паренхиматозных органов наблюдалось более резкое ухудшение тяжести болезни [36].
Факторы риска для тяжелой формы COVID-19 подробно обсуждаются в другом месте. (См. Coronavirus disease 2019 (COVID-19): Clinical features and diagnosis, раздел Risk factors for severe illness [англ.])
Эффект иммуносупрессии. Влияние иммуносупрессии на тяжесть течения COVID-19 у пациентов, подвергшихся трансплантации органов, остается неясным. Патогенез COVID-19, по-видимому, представляет собой взаимодействие между прямым вирус-опосредованным повреждением и ассоциированным ответом хозяина, при этом экспериментальные данные свидетельствуют о том, что дисрегуляция и гиперинтенсивный иммунный ответ могут опосредовать более тяжелое течение заболевания [37]. Поскольку иммуносупрессивные агенты модулируют несколько аспектов иммунного ответа хозяина, серьезность инфекции COVID-19 может потенциально зависеть от типа, комбинаций и интенсивности иммуносупрессии. Например, некоторые иммуносупрессивные препараты могут либо непосредственно (например, лимфоцит-истощающие антитела), либо косвенно (например, антиметаболиты) вызывать лимфопению, которая является зарегистрированным фактором риска для тяжелой формы COVID-19. Специфические агенты, независимо связанные со снижением иммунного ответа на вакцины (например, механистическая мишень ингибиторов рапамицина (mTOR), микофенолат), теоретически могут ослабить способность развивать адекватный иммунный ответ на естественную инфекцию. И наоборот, некоторые экспериментальные данные позволяют предположить, что ингибиторы mTOR могут обладать некоторой биологической активностью в отношении SARS-CoV-2 [38]. Необходимы дополнительные исследования, чтобы определить влияние специфических иммунодепрессантов на течение инфекции COVID-19.
Диагностика. Критерии для тестирования на COVID-19 у реципиентов паренхиматозных органов те же, что и у населения в целом. Однако в их случае у врачей должен быть более высокая настороженность в отношении инфекции, как это обычно рекомендуется для пациентов с ослабленным иммунитетом (Таблица 1).
- Пациентам с подозрением на COVID-19, госпитализированным для трансплантации, рекомендуется провести тестирование.
- Для реципиентов с легкими симптомами оптимальная практика не определена. В то время как некоторые одобряют тестирование всех таких пациентов, упирая на возможность быстрого прогрессирования заболевания, другие предпочитают ставить клинический диагноз и контролировать пациента на дому. Таким образом, решение часто принимается индивидуально по каждому случаю, на основе локальной распространенности COVID-19, доступных ресурсов и предпочтений пациента (См. "Coronavirus disease 2019 (COVID-19): Outpatient evaluation and management in adults", раздел 'Monoclonal antibodies and convalescent plasma therapy' [англ.])
- Рутинный скрининг бессимптомных реципиентов не рекомендуется.
Конкретные методы тестирования обсуждаются отдельно. (См. Coronavirus disease 2019 (COVID-19): Clinical features and diagnosis, раздел Clinical suspicion and criteria for testing [англ.])
Таблица 1. Диагностические исследования на COVID-19
* CDC рекомендует мазки из носоглотки, носовой полости (из области средней носовой раковины или преддверия носа), смывы из полости носа и носоглотки, мазки из ротоглотки, исследование слюны. Американское общество инфекционных болезней рекомендует мазок из носоглотки, из области средней носовой раковины, преддверия носа, исследование слюны или комбинацию мазка из преддверия носовой полости и ротоглотки. Это считается предпочтительнее мазка только из ротоглотки. Взятие мазка из носовой полости может быть выполнено больным самостоятельно в домашних условиях. Мазок из области средней носовой раковины и сбор слюны могут быть выполнены пациентами под наблюдением специалистов. Сбор образцов биоматериала из нижних дыхательных путей производится у госпитализированных пациентов с подозрением на инфекцию нижних дыхательных путей при отрицательных результатах исследований материалов из верхних дыхательных путей.
** В большинстве случаев однократный положительный результат подтверждает диагноз. Если при первом исследовании был получен отрицательный результат, однако уровень клинического подозрения остается высоким, рекомендовано проводить повторное тестирование.
*** Простые экспресс-тесты могут быть выполнены на месте, результат может быть получен в пределах 1 часа. При выполнении большинства более сложных лабораторных тестов для получения результата необходимо несколько часов. Однако время получения результата зависит от того, насколько часто тест выполняется, и ряда других факторов.
Тактика ведения
Общие подходы. Подход к лечению острой инфекции COVID-19 у реципиентов паренхиматозных органов такой же, как и при лечении остальных пациентов. Все специфические противовирусные препараты, используемые для лечения COVID-19, находятся в стадии изучения. Эти препараты, как правило, применяются только для лечения госпитализированных пациентов с тяжелой формой заболевания или с риском ее развития. По возможности лечение должно проводиться как часть клинического исследования.
Эти вопросы обсуждаются более подробно отдельно:
- См. "Coronavirus disease 2019 (COVID-19): Outpatient evaluation and management in adults" (англ.)
- См. Coronavirus disease 2019 (COVID-19): Management in hospitalized adults (англ.)
- См."Coronavirus disease 2019 (COVID-19): Clinical manifestations and diagnosis in children" (англ.)
- См. Coronavirus disease 2019 (COVID-19): Critical care and airway management issues (англ.)
Регулирование иммуносупрессии. Корректировка иммуносупрессивных схем должна быть определена индивидуально, исходя из тяжести заболевания, трансплантируемого органа, времени, прошедшего после трансплантации, а также риска острого отторжения аллотрансплантата [21, 24, 29, 39-41].
Хотя оптимальный подход не определен, мы обычно снижаем иммуносупрессию у пациентов, больных COVID-19 в форме от умеренной до тяжелой (например, нуждающихся в госпитализации).
- В качестве первого шага мы часто снижаем или удерживаем антиметаболит (например, микофенолат мофетила/натрия), особенно для пациентов с лимфопенией (например, когда абсолютное количество лимфоцитов < 700 кл/мл).
- Как правило, мы продолжаем применение ингибитора кальциневрина (CNI), поскольку CNI ингибирует интерлейкин (IL)-6 и IL-1, которые могут способствовать развитию тяжелого, нерегулируемого иммунного ответа, наблюдаемого у некоторых пациентов с тяжелой формой COVID-19.
- Основываясь на опыте с другими эпидемическими коронавирусами, мы, как правило, избегаем высоких доз глюкокортикоидов, так как эти агенты связаны с длительным выделением вируса и могут приводить к неблагоприятным исходам. (См. Coronavirus disease 2019 (COVID-19): Management in hospitalized adults, раздел Limited role of glucocorticoids [англ.])
Однако во всех случаях решение о снижении иммуносупрессии должно быть тщательно взвешено с учетом риска острого отторжения, особенно у реципиентов, которым обычно требуется высокий уровень поддерживающей иммуносупрессии (например, у реципиентов легких или сердца). Оптимальное ведение иммуносупрессивной терапии у реципиентов паренхиматозных органов с инфекцией COVID-19 неизвестно, и данные ограничиваются сообщениями о случаях и сериях случаев [21,22,24,29,42,43].
Также существуют опасения, что сама инфекция COVID-19 может повысить риск острого отторжения и что чрезмерно интенсивный воспалительный иммунный ответ хозяина может способствовать общей тяжести заболевания. Таким образом, ослабление иммунного ответа путем поддержания иммунодепрессии в низких дозах теоретически может быть полезным. Кроме того, экспериментальные данные свидетельствуют о том, что некоторые иммунодепрессанты, такие как ингибиторы mTOR, могут обладать биологической активностью в отношении SARS-CoV-2 [38]. Для подтверждения этих выводов необходимы дополнительные исследования.
Дополнительные рекомендации по регулированию иммуносупрессии у реципиентов трансплантата с активной инфекцией можно найти в следующих обзорах темы:
- См. Kidney transplantation in adults: Maintenance immunosuppressive therapy, раздел Patients who develop an infection [англ.])
- См. Maintenance immunosuppression following lung transplantation, раздел Monitoring and adjusting maintenance therapy [англ.])
- См. Coronavirus disease 2019 (COVID-19): Myocardial injury, раздел Cardiac transplantation [англ.])
Рекомендации от конкретных медицинских обществ перечислены отдельно — см. раздел «Ссылки на руководства».
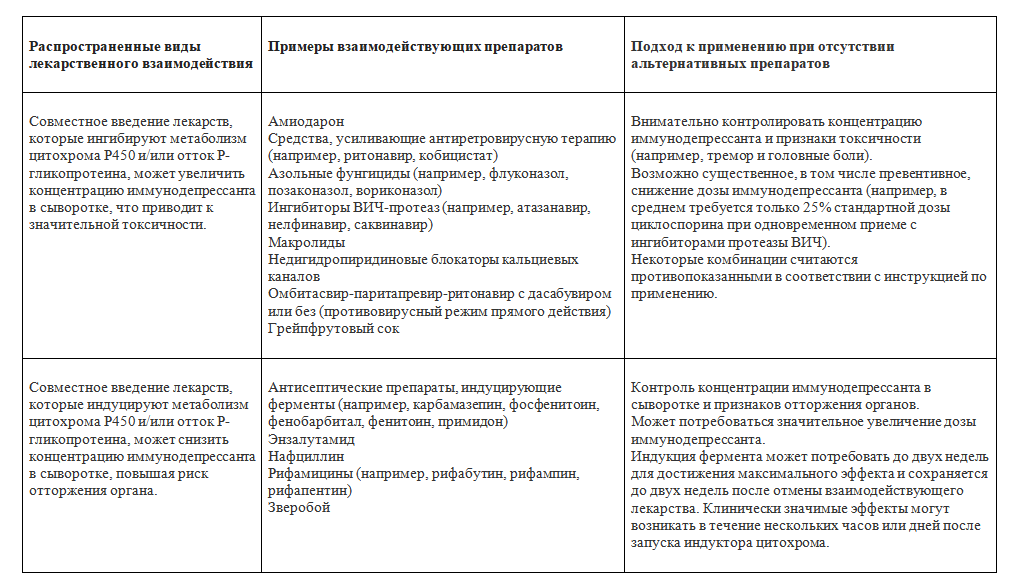
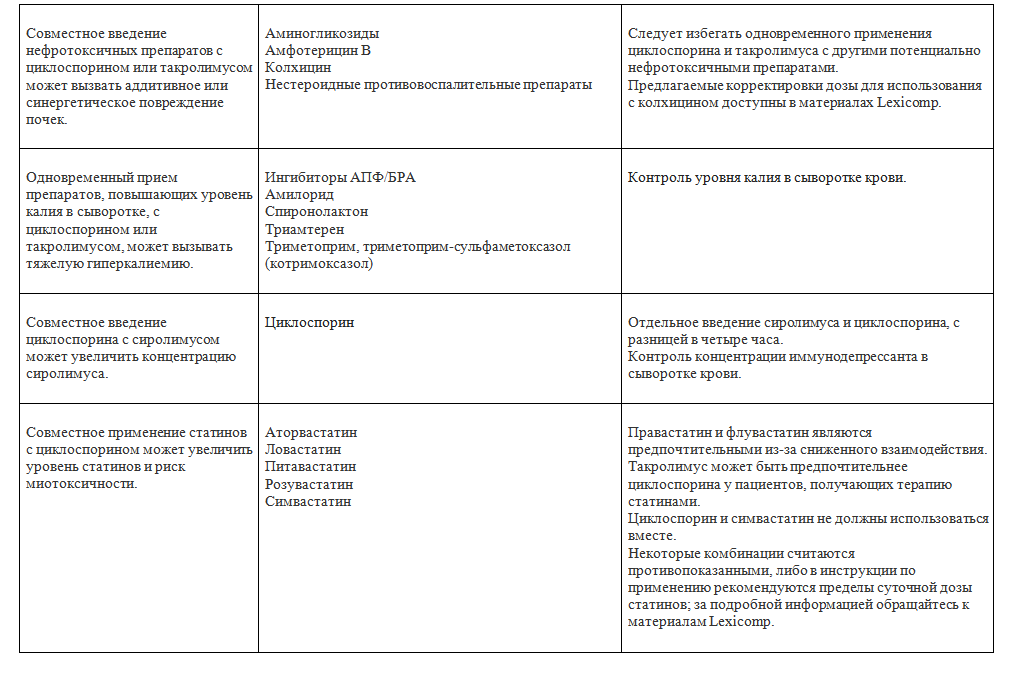
Лекарственные взаимодействия. Некоторые экспериментальные препараты, используемые для терапии COVID-19, потенциально могут вступить в лекарственные взаимодействия с препаратами, которые обычно используются для лечения реципиентов органов [44]. В частности, лекарства, которые удлиняют интервал QT (например, гидроксихлорохин, азитромицин), следует использовать с осторожностью, поскольку многие реципиенты паренхиматозных органов принимают CNI, что также может увеличить интервал QT. Кроме того, следует проявлять осторожность с ингибиторами протеазы (такими как лопинавир и ритонавир), которые могут снизить метаболизм и значительно повысить уровень CNI в крови (Таблица 2).
Таблица 2. Примеры лекарственных взаимодействий иммунодепрессантов, используемых при трансплантации органов: циклоспорина, такролимуса, сиролимуса и эверолимуса
Важное примечание: взаимодействия, перечисленные в этой таблице, иллюстрируют некоторые распространенные типы взаимодействий с иммунодепрессантами; это не полный список.
Циклоспорин, такролимус, сиролимус и эверолимус в значительной степени зависят от метаболизма цитохрома Р450 и также являются субстратами насоса P-гликопротеина. Некоторые взаимодействия могут привести к субтерапевтическим или опасно токсичным уровням концентрации иммунодепрессантов.
Когда подходящие невзаимодействующие альтернативы легко доступны, рассмотрите возможность модификации лечения, чтобы избежать комбинированного использования с мощными ингибиторами/индукторами метаболизма или агентами, которые, как известно, обладают аддитивной токсичностью с иммунодепрессантами.
Медикаментозная терапия должна проводиться специалистами по трансплантации, имеющими опыт терапевтического лекарственного мониторинга, а дозы следует корректировать на основе измерения концентрации иммунодепрессантов, особенно при изменении медикаментозной терапии. Если есть какие-либо сомнения в безопасности конкретного лекарства или добавки, их следует обсудить с центром трансплантации до начала лечения.
Ссылки на руководства
Ссылки на руководства из разных стран и регионов мира предоставлены отдельно. (См. Society guideline links: Coronavirus disease 2019 (COVID-19) – International and government guidelines for general care, Society guideline links: Coronavirus disease 2019 (COVID-19) – Guidelines for specialty care и Society guideline links: Coronavirus disease 2019 (COVID-19) – Resources for patients [англ.])
Информация для пациентов
UpToDate предлагает два типа учебных материалов для пациентов: The Basics и Beyond the Basics. The Basics написаны на простом языке, на уровне пятого-шестого класса, и отвечают на четыре-пять ключевых вопросов о том или ином состоянии. Эти статьи лучше всего подходят для пациентов, которым нужен общий обзор и которые предпочитают короткие, удобные для чтения материалы. В Beyond the Basics материалы для пациентов более длинные, сложные и подробные. Эти статьи написаны на уровне старших классов и подходят пациентам, которые хотят углубиться в тему и знакомы с медицинской терминологией.
Статья для пациентов о COVID-19, написанная на базовом уровне, доступна здесь (на английском языке): Patient education: Coronavirus disease 2019 (COVID-19) overview (The Basics).
Резюме и рекомендации
- COVID-19 ставит новые задачи перед кандидатами на трансплантацию и реципиентами, а также перед самим процессом трансплантации органов. (См. «Введение».)
- Существует теоретический риск передачи SARS-CoV-2 (вируса, который вызывает COVID-19) от донора органов реципиенту, основанный на обнаружении вирусной РНК в органах, которые могут быть трансплантированы (например, в легких, сердце, почках, кишечнике), хотя донорские инфекции не были зарегистрированы до настоящего времени. (См. «Вероятность донорской инфекции».)
- Из-за этого риска и возможности передачи SARS-CoV-2 медицинским работникам все доноры органов и кандидаты на трансплантацию должны быть проверены на наличие COVID-19 с помощью тщательного сбора анамнеза, визуализации органов грудной клетки и микробиологического тестирования. (См. «Скрининг перед трансплантацией».)
- После трансплантации реципиенты органов могут подвергаться повышенному риску заболеть COVID-19, потому что они имеют ослабленный иммунитет и часто контактируют с системой здравоохранения, хотя эта связь не изучалась. (См. «Посттрансплантационный риск».)
- Клинические проявления COVID-19 у реципиентов органов различны и сходны с таковыми у пациентов с ослабленным иммунитетом. Является ли течение болезни более тяжелым, неизвестно. (См. «Клиническая картина» и «Тяжесть заболевания».)
- Подход к диагностике аналогичен подходу для населения в целом. Поскольку признаки и симптомы COVID-19 у реципиентов трансплантата могут быть едва различимыми, а прогрессирование заболевания — быстрым, у некоторых врачей более низкий порог для оценки и тестирования реципиентов. (См. «Диагностика».)
- Подход к лечению (например, использование противовирусных препаратов, поддерживающая терапия) также аналогичен подходу для населения в целом, хотя следует уделять пристальное внимание потенциальным лекарственным взаимодействиям и воздействию на иммуносупрессивный режим. (См. «Общие соображения» и «Лекарственное взаимодействие».)
- Корректировки иммуносупрессивного режима должны определяться индивидуально, исходя из тяжести заболевания, вида трансплантируемого органа, времени после трансплантации и риска острого отторжения аллотрансплантата. (См. «Регулирование иммуносупрессии».)
Ссылки
- Wang W, Xu Y, Gao R, et al. Detection of SARS-CoV-2 in Different Types of Clinical Specimens. JAMA 2020; 323:1843.
- Tavazzi G, Pellegrini C, Maurelli M, et al. Myocardial localization of coronavirus in COVID-19 cardiogenic shock. Eur J Heart Fail 2020; 22:911.
- Bo Diao, Chenhui Wang, Rongshuai Wang, et al. Human Kidney is a Target for Novel Severe Acute Respiratory Syndrome Coronavirus 2 (SARS-CoV-2) Infection. medRxIv. This article is preprint and has not been peer-reviewed. https://doi.org/10.1101/2020.03.04.20031120.
- Huang C, Wang Y, Li X, et al. Clinical features of patients infected with 2019 novel coronavirus in Wuhan, China. Lancet 2020; 395:497.
- Chang L, Yan Y, Wang L. Coronavirus Disease 2019: Coronaviruses and Blood Safety. Transfus Med Rev 2020; 34:75.
- Organ retrieval for transplantation in the COVID-19 era. American Society of Transplant Surgeons. https://asts.org/advocacy/covid-19-resources/asts-covid-19-strike-force/asts-covid-19-strike-force-organ-retrieval-guidance#.Xqb1BGhKiUl (Accessed on April 26, 2020).
- Loupy A, Aubert O, Reese PP, et al. Organ procurement and transplantation during the COVID-19 pandemic. Lancet 2020; 395:e95.
- Lentine KL, Vest LS, Schnitzler MA, et al. Survey of US Living Kidney Donation and Transplantation Practices in the COVID-19 Era. Kidney Int Rep 2020; 5:1894.
- Ahn C, Amer H, Anglicheau D, et al. Global Transplantation COVID Report March 2020. Transplantation 2020; 104:1974.
- Ahmed O, Brockmeier D, Lee K, et al. Organ donation during the COVID-19 pandemic. Am J Transplant 2020; 20:3081.
- Boyarsky BJ, Werbel WA, Durand CM, et al. Early national and center-level changes to kidney transplantation in the United States during the COVID-19 epidemic. Am J Transplant 2020; 20:3131.
- Non-emergent, elective medical services, and treatment recommendations. Centers for Medicare & Medicaid Services. https://www.cms.gov/files/document/cms-non-emergent-elective-medical-recommendations.pdf (Accessed on April 26, 2020).
- Craig-Schapiro R, Salinas T, Lubetzky M, et al. COVID-19 outcomes in patients waitlisted for kidney transplantation and kidney transplant recipients. Am J Transplant 2020.
- Massie AB, Boyarsky BJ, Werbel WA, et al. Identifying scenarios of benefit or harm from kidney transplantation during the COVID-19 pandemic: A stochastic simulation and machine learning study. Am J Transplant 2020; 20:2997.
- American Society for Transplantation. Information for transplant professionals and community members regarding 2019 novel coronavirus. https://www.myast.org/sites/default/files/1COVID19%20FAQ%20Tx%20Centers%2004.15.2020.pdf (Accessed on April 18, 2020).
- SARS-CoV-2 (Coronavirus, 2019-nCoV): Recommendations and guidance for organ donor testing. American Society of Transplantation. http://www.myast.org/sites/default/files/Donor%20Testing_100520_revised_ReadyToPostUpdated10-12.pdf (Accessed on November 29, 2020).
- Zhou F, Yu T, Du R, et al. Clinical course and risk factors for mortality of adult inpatients with COVID-19 in Wuhan, China: a retrospective cohort study. Lancet 2020; 395:1054.
- Man Z, Jing Z, Huibo S, et al. Viral shedding prolongation in a kidney transplant patient with COVID-19 pneumonia. Am J Transplant 2020; 20:2626.
- Zhu L, Gong N, Liu B, et al. Coronavirus Disease 2019 Pneumonia in Immunosuppressed Renal Transplant Recipients: A Summary of 10 Confirmed Cases in Wuhan, China. Eur Urol 2020; 77:748.
- Guillen E, Pineiro GJ, Revuelta I, et al. Case report of COVID-19 in a kidney transplant recipient: Does immunosuppression alter the clinical presentation? Am J Transplant 2020; 20:1875.
- Pereira MR, Mohan S, Cohen DJ, et al. COVID-19 in solid organ transplant recipients: Initial report from the US epicenter. Am J Transplant 2020; 20:1800.
- Akalin E, Azzi Y, Bartash R, et al. Covid-19 and Kidney Transplantation. N Engl J Med 2020; 382:2475.
- Tschopp J, L'Huillier AG, Mombelli M, et al. First experience of SARS-CoV-2 infections in solid organ transplant recipients in the Swiss Transplant Cohort Study. Am J Transplant 2020; 20:2876.
- Caillard S, Anglicheau D, Matignon M, et al. An initial report from the French SOT COVID Registry suggests high mortality due to COVID-19 in recipients of kidney transplants. Kidney Int 2020; 98:1549.
- Roberts MB, Izzy S, Tahir Z, et al. COVID-19 in solid organ transplant recipients: Dynamics of disease progression and inflammatory markers in ICU and non-ICU admitted patients. Transpl Infect Dis 2020; 22:e13407.
- Fishman JA. The Immunocompromised Transplant Recipient and SARS-CoV-2 Infection. J Am Soc Nephrol 2020; 31:1147.
- Fernández-Ruiz M, Andrés A, Loinaz C, et al. COVID-19 in solid organ transplant recipients: A single-center case series from Spain. Am J Transplant 2020; 20:1849.
- Crespo M, Pérez-Sáez MJ, Redondo-Pachón D, et al. COVID-19 in elderly kidney transplant recipients. Am J Transplant 2020; 20:2883.
- Kates OS, Haydel BM, Florman SS, et al. COVID-19 in solid organ transplant: A multi-center cohort study. Clin Infect Dis 2020.
- Aversa M, Benvenuto L, Anderson M, et al. COVID-19 in lung transplant recipients: A single center case series from New York City. Am J Transplant 2020; 20:3072.
- Cravedi P, Mothi SS, Azzi Y, et al. COVID-19 and kidney transplantation: Results from the TANGO International Transplant Consortium. Am J Transplant 2020; 20:3140.
- Bossini N, Alberici F, Delbarba E, et al. Kidney transplant patients with SARS-CoV-2 infection: The Brescia Renal COVID task force experience. Am J Transplant 2020; 20:3019.
- Favà A, Cucchiari D, Montero N, et al. Clinical characteristics and risk factors for severe COVID-19 in hospitalized kidney transplant recipients: A multicentric cohort study. Am J Transplant 2020; 20:3030.
- Molnar MZ, Bhalla A, Azhar A, et al. Outcomes of critically ill solid organ transplant patients with COVID-19 in the United States. Am J Transplant 2020; 20:3061.
- Avery RK. COVID-19 Therapeutics for Solid Organ Transplant Recipients; 6 Months Into the Pandemic: Where Are We Now? Transplantation 2021; 105:56.
- Avery RK, Chiang TP, Marr KA, et al. Inpatient COVID-19 Outcomes in Solid Organ Transplant Recipients Compared to Non-Solid Organ Transplant Patients: A Retrospective Cohort. Am J Transplant 2020.
- Chen G, Wu D, Guo W, et al. Clinical and immunological features of severe and moderate coronavirus disease 2019. J Clin Invest 2020; 130:2620.
- Conti P, Ronconi G, Caraffa A, et al. Induction of pro-inflammatory cytokines (IL-1 and IL-6) and lung inflammation by Coronavirus-19 (COVI-19 or SARS-CoV-2): anti-inflammatory strategies. J Biol Regul Homeost Agents 2020; 34:327.
- Latif F, Farr MA, Clerkin KJ, et al. Characteristics and Outcomes of Recipients of Heart Transplant With Coronavirus Disease 2019. JAMA Cardiol 2020.
- Yi SG, Rogers AW, Saharia A, et al. Early Experience With COVID-19 and Solid Organ Transplantation at a US High-volume Transplant Center. Transplantation 2020; 104:2208.
- Nair V, Jandovitz N, Hirsch JS, et al. COVID-19 in kidney transplant recipients. Am J Transplant 2020; 20:1819.
- Zhong Z, Zhang Q, Xia H, et al. Clinical characteristics and immunosuppressant management of coronavirus disease 2019 in solid organ transplant recipients. Am J Transplant 2020; 20:1916.
- Banerjee D, Popoola J, Shah S, et al. COVID-19 infection in kidney transplant recipients. Kidney Int 2020; 97:1076.
- Elens L, Langman LJ, Hesselink DA, et al. Pharmacologic Treatment of Transplant Recipients Infected With SARS-CoV-2: Considerations Regarding Therapeutic Drug Monitoring and Drug-Drug Interactions. Ther Drug Monit 2020; 42:360.