Блокаторы ренин – ангиотензин – альдостероновой системы и риск развития COVID-19

Тип: Статья
Автор: Giuseppe Mancia et al.
Опубликовано: The new England journal of medicine 01.05.2020
Перевод: Анна Шестакова, Фонд профилактики рака
Аннотация
Актуальность исследования
Потенциальная связь между использованием блокаторов рецепторов ангиотензина (БРА) и ингибиторов ангиотензинпревращающего фермента (АПФ) и риском развития коронавирусной болезни 2019 (COVID-19) была изучена недостаточно хорошо.
Методы исследования
Мы провели популяционное исследование случай-контроль в итальянском регионе Ломбардия. В общей сложности мы сопоставили 6272 пациентов, у которых инфекция, вызванная вирусом SARS-CoV-2, подтверждена в период с 21 февраля по 11 марта 2020 года, с 30 759 бенефициарами Региональной службы здравоохранения (контроли) по полу, возрасту и муниципалитету проживания. Информацию об использовании отдельных лекарственных препаратов и клинические данные пациентов мы получили из региональных баз данных об использовании медицинских услуг. Коэффициенты шансов и 95% доверительные интервалы для связей между препаратами и инфекцией с поправкой на искажающие результаты факторы мы оценили с помощью логистической регрессии.
Результаты исследования
Средний возраст пациентов (± стандартное отклонение) составлял 68 ± 13 лет, из них 37% — женщины. Ингибиторы АПФ и БРА, так же как и другие антигипертензивные и не антигипертензивные препараты чаще использовали пациенты с заболеванием, чем контрольная группа, также эти пациенты имели худший клинический профиль. Использование БРА или ингибиторов АПФ не выявило какой-либо связи с COVID-19 среди пациентов в целом (скорректированное отношение шансов, составило 0,95 [95% доверительный интервал {ДИ}, 0,86-1,05] для БРА и 0,96 [95% ДИ, 0,87-1,07] для ингибиторов АПФ) и среди пациентов с тяжелым или смертельным течением заболевания (скорректированное отношение шансов 0,83 [95% ДИ, 0,63-1,10] для БРА и 0,91 [95% ДИ, 0,69-1,21] для ингибиторов АПФ), не обнаружено связи между этими переменными по полу.
Заключение
Ингибиторы АПФ и БРА чаще использовали пациенты с COVID-19, потому что в этой группе более распространены сердечно-сосудистые заболевания. Тем не менее, нет доказательств, что ингибиторы АПФ или БРА влияют на риск развития COVID-19.
Результаты исследования
Случаи пациентов и контрольные
Из 6292 пациентов для 20 человек не был найден контрольный случай того же самого пола, возраста и города проживания. Оставшихся 6272 пациентов (99,7%), которые были включены в анализ, сопоставили с 30 759 контрольными. Сопоставление 1 : 5 было полностью успешным для 6015 включенных пациентов, в то время как для остальных 257 пациентов (менее 4,1%) было доступно менее 5 контролей. На индексную дату средний возраст пациентов (± SD) и контрольных пациентов составлял 68 ± 13 лет, почти 37% из них — женщины (соответствующие переменные).
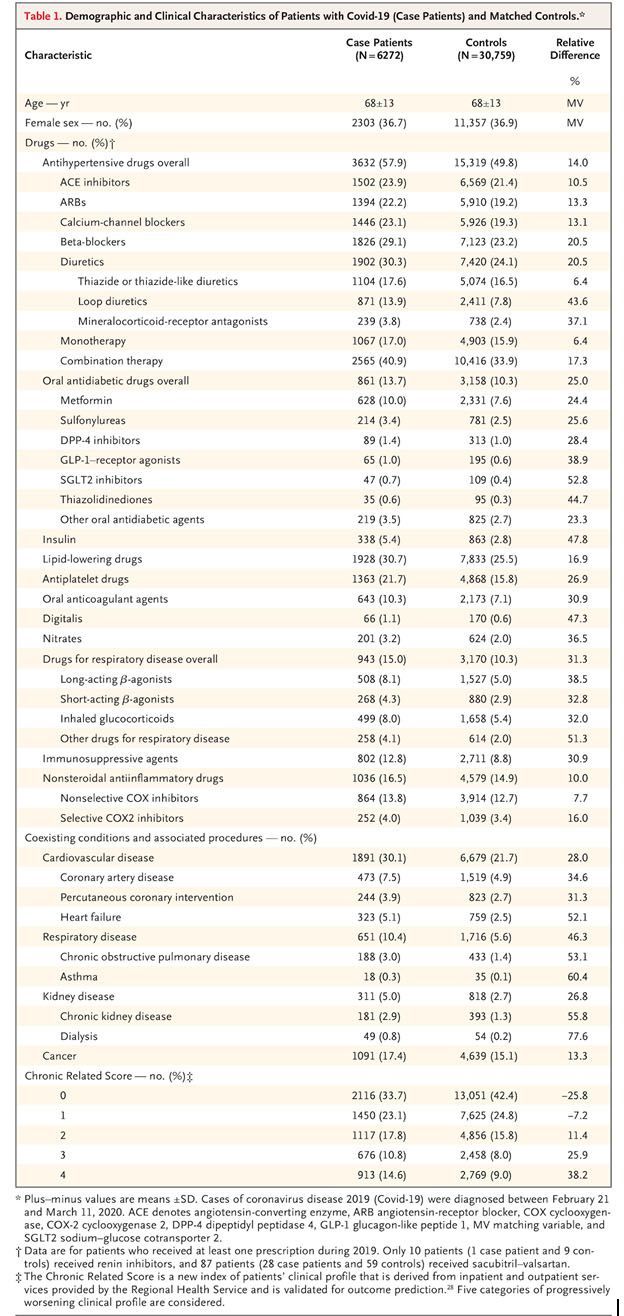
В таблице 1 показано, что БРА и ингибиторы АПФ чаще назначались пациентам, чем контрольной группе. Процент пациентов, получавших БРА, составлял 22,2% среди пациентов с заболеванием и 19,2% среди пациентов контрольной группы (относительная разница - 13,3%); процент пациентов, получавших ингибиторы АПФ, составил 23,9% и 21,4% соответственно (относительная разница 10,5%). Другие антигипертензивные препараты также чаще использовали пациенты, чем контрольная группа, разница обычно была больше, чем у ингибиторов АПФ и БРА, особенно для петлевых диуретиков (13,9% против 7,8%; относительная разница 43,6%) и антагонистов минералокортикоидных рецепторов (3,8% против 2,4%; относительная разница 37,1%). Применение ингибиторов ренина (1 пациент) и сакубитрил-валсартан (28 пациентов) было редкостью, и дальнейший анализ этих методов лечения не проводился. Пациенты также использовали комбинацию антигипертензивных препаратов чаще, чем контрольные, имели более частую историю госпитализаций по поводу сердечно-сосудистых и не сердечно-сосудистых заболеваний и, согласно индексу CReSc (прим. Chronic Related Score), имели в целом существенно худший клинический профиль.
Блокаторы рецепторов ангиотензина, ингибиторы ангиотензинпревращающего фермента и COVID-19
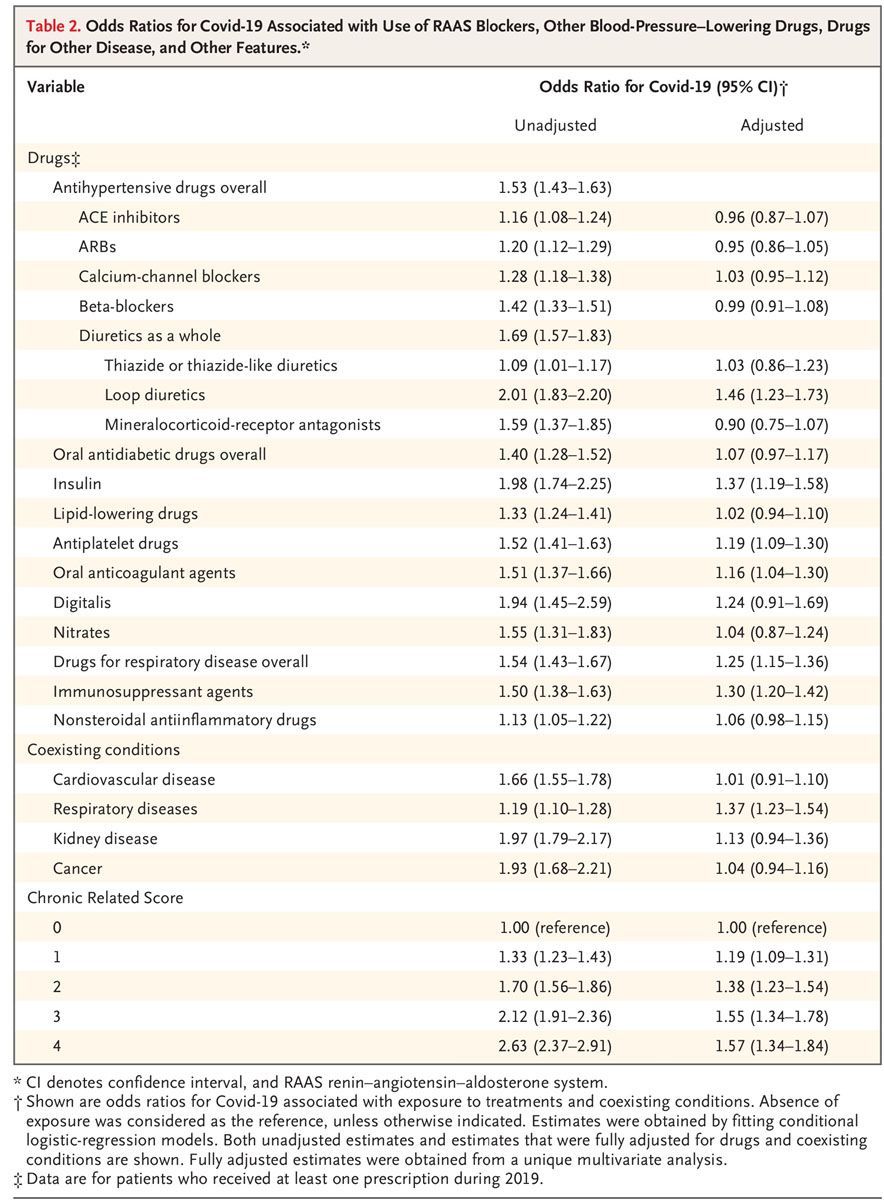
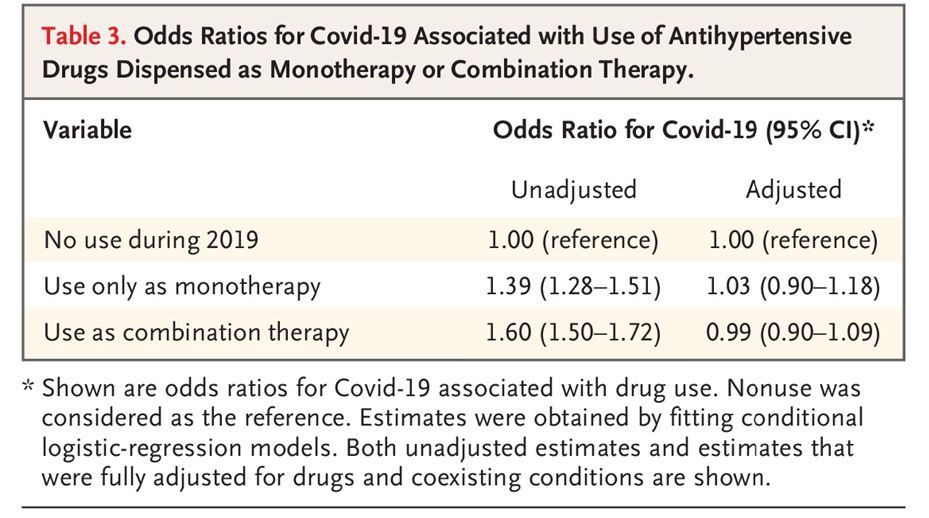
В таблице 2 приведены нескорректированные оценки риска COVID-19 в соответствии с препаратами, показанными в таблице 1, что предполагает возможный эффект. Однако после многопараметрической коррекции ни БРА, ни ингибиторы АПФ не имели значительной связи с риском COVID-19. Это также относится к блокаторам кальциевых каналов, бета-блокаторам и диуретикам. Связь с COVID-19 после многопараметрической коррекции поддерживалась петлевыми диуретиками и некоторыми другими препаратами (инсулин, антиагреганты, антикоагулянты, иммунодепрессанты и препараты, применяемые при заболеваниях дыхательных путей). По сравнению с пациентами, которые не использовали антигипертензивные препараты в течение 2019 года, те, кому антигипертензивные препараты вводили в виде монотерапии или комбинации двух или более препаратов, имели больший риск COVID-19 в нескорректированном (грубом) анализе. Но после многопараметрической коррекции ни монотерапия, ни комбинированная терапия не показали значимой связи с риском COVID-19 (Таблица 3). Многовариантный скорректированный риск COVID-19 был увеличен у пациентов с предыдущими госпитализациями по поводу сердечно-сосудистых или не сердечно-сосудистых заболеваний. Он также постепенно увеличивался по мере увеличения CReSc (Таблица 2).
Подгруппа и анализ чувствительности
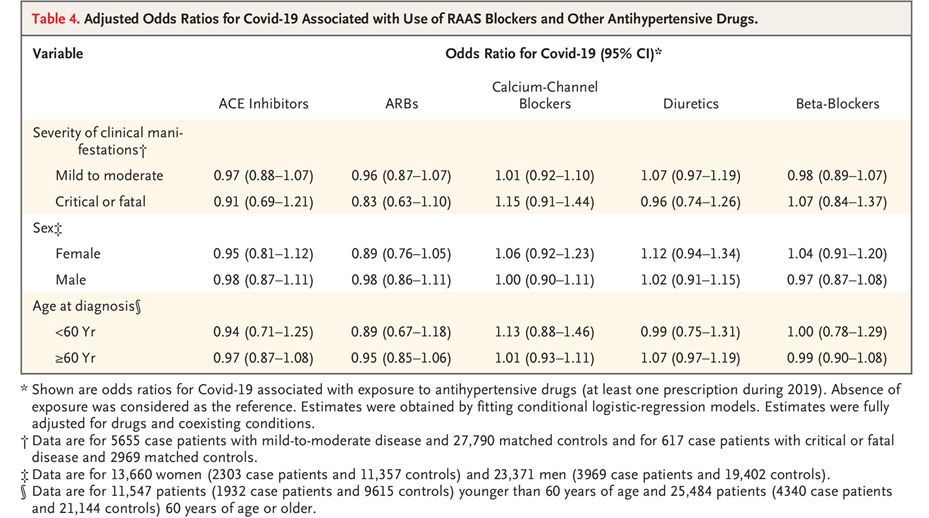
Данные о риске COVID-19, связанном с применением блокаторов РААС и других препаратов, были одинаковыми у мужчин и женщин (таблица 4 и таблицы S2 и S3). Не было статистических доказательств, что результаты, полученные для всей когорты, варьировались в зависимости от возраста или тяжести клинических проявлений и течения COVID-19 (Таблица 4 и таблицы S3-S5). Как показано на рисунке S1, данные по COVID-19 и антигипертензивным препаратам были согласованы независимо от того, оценивалось ли употребление препаратов по свободным или более строгим критериям. Кроме того, результаты существенно не изменились, когда пациенты случая были стратифицированы согласно дате диагноза COVID-19 (Таблица S6).
Обсуждение результатов
В этом исследовании БРА и ингибиторы АПФ чаще использовали пациенты, инфицированные SARS-CoV-2, чем большое число контрольной группы, сопоставимой по возрасту, полу и месту проживания. Тем не менее все другие основные антигипертензивные препараты, такие как блокаторы кальциевых каналов, бета-блокаторы и диуретики, также чаще использовали пациенты с COVID-19, и их отличия от контроля были больше, чем показанные для БРА и ингибиторов АПФ. Кроме того, в многопараметрическом анализе, в котором данные были скорректированы для ряда связанных с лечением сопутствующих переменных и маркеров клинического состояния пациента, использование БРА или ингибиторов АПФ не было в значительной степени связано с риском развития COVID-19. Наконец, не было статистических доказательств независимой связи между использованием комбинации антигипертензивных препаратов (в которых ингибитор АПФ или БРА является наиболее распространенным компонентом) и риском COVID-19. Таким образом, наши результаты не дают доказательств независимой связи между блокаторами РААС и восприимчивостью к SARS-CoV-2 у людей.
Мы обнаружили, что у пациентов с COVID-19 была более высокая базовая распространенность сердечно-сосудистых состояний и заболеваний (гипертония, ишемическая болезнь сердца, сердечная недостаточность и хроническая болезнь почек), которые часто лечат изученными здесь препаратами. Такие результаты подтверждают предыдущие наблюдения китайских исследователей о том, что пациенты с COVID-19, как правило, имеют худшее здоровье, чем население в целом, [11-15], и вывод, что пациенты с COVID-19 чаще лечились препаратами от многих не сердечно-сосудистых заболеваний, имели более высокую частоту предыдущих госпитализаций по разным причинам и более высокие показатели хронических сопутствующих состояний, чем контрольные случаи. [6,29,30]
Настоящее исследование предоставляет несколько дополнительных выводов. Во-первых, вывод о том, что блокаторы РААС не модифицируют восприимчивость к COVID-19, применим к обоим полам, а также к более молодым и пожилым людям. Во-вторых, наши данные не дают доказательств, что вместо изменения восприимчивости к COVID-19 блокаторы РААС изменяют развитие заболевания, то есть влияют на его тяжесть. В нашем исследовании ни ингибиторы АПФ, ни БРА не показали независимой связи с COVID-19 у пациентов с легкой-умеренной тяжестью или с тяжелым течением заболевания. В-третьих, пациенты с COVID-19 более часто использовали петлевые диуретики и антагонисты минералокортикоидных рецепторов, чем контрольные случаи, и лечение с помощью петлевых диуретиков было связано с повышенным риском COVID-19 в многопараметрическом анализе. Вместо того, чтобы предлагать корреляцию (для которой нет механистической поддержки), этот вывод, вероятно, будет означать, что использование петлевых диуретиков отражает наличие клинических состояний, таких как сердечная недостаточность или прогрессирующее повреждение почек, степень тяжести которых не была должным образом определена доступными клиническими данными и оценками. Эти наблюдения из нашего исследования могут объяснять независимую связь между COVID-19 и некоторыми не сердечно-сосудистыми препаратами, хотя для выяснения этой проблемы потребуются более прямые исследования с соответствующими экспериментальными схемами.
Одна из сильных сторон исследования заключается в большом количестве пациентов, а также в большой и хорошо подобранной контрольной группе, без которой интерпретация собранных данных была бы затруднительной. Еще одно преимущество в том, что база данных Ломбардии включала предыдущие госпитализации и позволяла точно соблюдать предписанные для амбулаторных пациентов лекарства, поскольку фармацевты должны подавать амбулаторные рецепты для получения компенсации, а неправильные отчеты влекут за собой юридические последствия.
Ограничения исследования: информация о применении лекарственных препаратов ограничивается рецептами, а фактическое потребление лекарств пациентами и контрольными пациентами не может быть оценено. Медикаменты, которые были приобретены пациентами (поскольку врачи выписывали их в частном порядке, а в Национальной системе здравоохранения не было записей), а также лекарства, отпускаемые после 31 декабря 2019 года, не были учтены в нашем анализе. Тем не менее, антигипертензивные препараты редко покупают за свой счет, так как их выписывают бесплатно. И предварительный анализ, включающий пациентов, у которых антигипертензивное лечение проводилось регулярно или ближе к моменту заражения, не изменил результаты. Наши результаты отражают дозы блокаторов РААС, используемые в итальянской медицинской практике, но не позволяют нам исследовать другие дозы, поскольку этой информации нет в базе данных. Вполне вероятно, что в контрольную группу входило несколько человек с COVID-19, поскольку население Италии в целом не проходило тестирование. Неизмеримые, искажающие результаты факторы могли быть ответственны за наши выводы. Например, учитывая гипотезу о том, что блокаторы РААС увеличивают риск тяжелых клинических проявлений COVID-19, блокаторы РААС могут предпочтительно выдавать пациентам с лучшими клиническими характеристиками и более низкой предполагаемой вероятностью развития тяжелого COVID-19. Тем не менее не было доказательств, что пациенты, которые получали БРА или ингибиторы АПФ, имели лучший клинический профиль, чем те, кто получал другие антигипертензивные препараты. Наконец, наши результаты применимы к большей части белого населения и не могут быть обобщены для других рас.
Настоящее исследование не предоставляет доказательств, что использование ингибиторов АПФ или БРА независимо связано с риском COVID-19.
Table 1. Demographic and Clinical Characteristics of Patients with Covid-19 (Case Patients) and Matched Controls.
Table 2. Odds Ratios for Covid-19 Associated with Use of RAAS Blockers, Other Blood-Pressure–Lowering Drugs, Drugs for Other Disease, and Other Features.
Table 3. Odds Ratios for Covid-19 Associated with Use of Antihypertensive Drugs Dispensed as Monotherapy or Combination Therapy.
Table 4. Adjusted Odds Ratios for Covid-19 Associated with Use of RAAS Blockers and Other Antihypertensive Drugs.
Ссылки
- Paul M, Poyan Mehr A, Kreutz R. Physiology of local renin-angiotensin systems. Physiol Rev 2006;86:747-803.
- Li W, Moore MJ, Vasilieva N, et al. Angiotensin-converting enzyme 2 is a functional receptor for the SARS coronavirus. Nature 2003;426:450-454.
- Zhou P, Yang XL, Wang XG, et al. A pneumonia outbreak associated with a new coronavirus of probable bat origin. Nature 2020;579:270-273.
- Soler MJ, Barrios C, Oliva R, Batlle D. Pharmacologic modulation of ACE2 expression. Curr Hypertens Rep 2008;10:410-414.
- Ferrario CM, Jessup J, Chappell MC, et al. Effect of angiotensin-converting enzyme inhibition and angiotensin II receptor blockers on cardiac angiotensin-converting enzyme 2. Circulation 2005;111:2605-2610.
- Fang L, Karakiulakis G, Roth M. Are patients with hypertension and diabetes mellitus at increased risk for COVID-19 infection? Lancet Respir Med 2020;8(4):e21-e21.
- Esler M, Esler D. Can angiotensin receptor-blocking drugs perhaps be harmful in the COVID-19 pandemic? J Hypertens 2020;38:781-782.
- Vaduganathan M, Vardeny O, Michel T, McMurray JJV, Pfeffer MA, Solomon SD. Renin–angiotensin–aldosterone system inhibitors in patients with Covid-19. N Engl J Med 2020;382:1653-1659.
- Danser AHJ, Epstein M, Batlle D. Renin-angiotensin system blockers and the COVID-19 pandemic. Hypertension 2020 March 25 (Epub ahead of print).
- Liu C-L, Shau W-Y, Wu C-S, Lai M-S. Angiotensin-converting enzyme inhibitor/angiotensin II receptor blockers and pneumonia risk among stroke patients. J Hypertens 2012;30:2223-2229.
- Shi S, Qin M, Shen B, et al. Association of cardiac injury with mortality in hospitalized patients with COVID-19 in Wuhan, China. JAMA Cardiol 2020 March 25 (Epub ahead of print).
- Guo T, Fan Y, Chen M, et al. Cardiovascular implications of fatal outcomes of patients with coronavirus disease 2019 (COVID-19). JAMA Cardiol 2020 March 27 (Epub ahead of print).
- Zhou F, Yu T, Du R, et al. Clinical course and risk factors for mortality of adult inpatients with COVID-19 in Wuhan, China: a retrospective cohort study. Lancet 2020;395:1054-1062.
- Chen N, Zhou M, Dong X, et al. Epidemiological and clinical characteristics of 99 cases of 2019 novel coronavirus pneumonia in Wuhan, China: a descriptive study. Lancet 2020;395:507-513.
- Guan W, Ni Z, Hu Y, et al. Clinical characteristics of coronavirus disease 2019 in China. N Engl J Med 2020;382:1708-1720.
- Kuster GM, Pfister O, Burkard T, et al. SARS-CoV2: should inhibitors of the renin-angiotensin system be withdrawn in patients with COVID-19? Eur Heart J 2020 March 20 (Epub ahead of print).
- HFSA/ACC/AHA statement addresses concerns re: using RAAS antagonists in COVID-19. Science News. April 10, 2020
- Patel AB, Verma A. COVID-19 and angiotensin-converting enzyme inhibitors and angiotensin receptor blockers: what is the evidence? JAMA 2020 March 24 (Epub ahead of print).
- Kreutz R, Algharably EAE, Azizi M, et al. Hypertension, the renin-angiotensin system, and the risk of lower respiratory tract infections and lung injury: implications for COVID-19. Cardiovasc Res 2020 April 15 (Epub ahead of print).
- Hirakawa Y, Arima H, Webster R, et al. Risks associated with permanent discontinuation of blood pressure-lowering medications in patients with type 2 diabetes. J Hypertens 2016;34:781-787.
- Halliday BP, Wassall R, Lota AS, et al. Withdrawal of pharmacological treatment for heart failure in patients with recovered dilated cardiomyopathy (TRED-HF): an open-label, pilot, randomised trial. Lancet 2019;393:61-73.
- Vardeny O, Claggett B, Kachadourian J, et al. Incidence, predictors, and outcomes associated with hypotensive episodes among heart failure patients receiving sacubitril/valsartan or enalapril: the PARADIGM-HF Trial (Prospective Comparison of Angiotensin Receptor Neprilysin Inhibitor With Angiotensin-Converting Enzyme Inhibitor to Determine Impact on Global Mortality and Morbidity in Heart Failure). Circ Heart Fail 2018;11(4):e004745-e004745.
- Coronavirus emergency. Rome: Department of Civil Protection
- Rea F, Corrao G, Merlino L, Mancia G. Early cardiovascular protection by initial two-drug fixed-dose combination treatment vs. monotherapy in hypertension. Eur Heart J 2018;39:3654-3661.
- Corrao G, Mancia G. Generating evidence from computerized healthcare utilization databases. Hypertension 2015;65:490-498.
- Corrao G, Rea F, Ghirardi A, Soranna D, Merlino L, Mancia G. Adherence with antihypertensive drug therapy and the risk of heart failure in clinical practice. Hypertension 2015;66:742-749.
- Corman VM, Landt O, Kaiser M, et al. Detection of 2019 novel coronavirus (2019-nCoV) by real-time RT-PCR. Euro Surveill 2020;25(3):2000045-2000045.
- Rea F, Corrao G, Ludergnani M, Cajazzo L, Merlino L. A new population-based risk stratification tool was developed and validated for predicting mortality, hospital admissions, and health care costs. J Clin Epidemiol 2019;116:62-71.
- Onder G, Rezza G, Brusaferro S. Case-fatality rate and characteristics of patients dying in relation to COVID-19 in Italy. JAMA 2020 March 23 (Epub ahead of print).
- Zheng Y-Y, Ma Y-T, Zhang J-Y, Xie X. COVID-19 and the cardiovascular system. Nat Rev Cardiol 2020;17:259-260.